Омоложение через эпигенетические механизмы на клеточном уровне через эпифизарно-тимусную иммунную ось
Статья - глава из книги-рукописи Гарбузова Г.А.: НЕОТЕНИЯ. ПРОДЛЕНИЕ МОЛОДОСТИ
Стареющая иммунная система как стартер для появления сенесцентных клеток
За отправную точку для решения вопроса возьмём мнение ряда работ, что если бы вилочковая железа работала всегда на 100 %, то мы бы постоянно находились в каком-то определённом возрасте, например, юности. В основе концепта автора лежит положение о том, что тимус отвечает за поддержку ювентальности* клеток, а точнее за сохранение и активность стволовых клеток. С инволюцией тимуса уровень генерации стволовых клеток падает.
Основные органы, где нахождение и активность стволовых клеток максимальна:
- селезёнка;
- костный мозг;
- спинной мозг;
- яичник у женщин, придатки яичек — у мужчин.
Степень участия у всех одинакова.
Однако же командует этим производством только вилочковая железа. По мере уменьшения энергетики эфирного органа тимуса его команды со временем слабеют.
Регулировки в организме осуществляются двухэтажно. Эпифиз и мелатонин поддерживают юность всех иммунных клеток. Но автор предлагает концепт о наличии общей стороны эпифизарно-тимусной иммунной системы для поддержания ювенильности. Согласно исследованиям, молодые иммунные клетки противодействуют старению организма, в то время как сенесцентные иммунные клетки, наоборот, способствуют этому процессу [1].
Удаление тимуса ускоряет старение организма. После удаления органа риск смерти от различных причин повышается почти в три раза [2]. В молодости тимус поддерживает ювентал клеток, а в более зрелом возрасте противодействует аутоиммунным, раковым и анизомалийным заболеваниям. Удаление тимуса, согласно исследованиям, происходило на взрослых людях, когда размеры тимуса уменьшены в десятки раз. Это говорит о том, что у тимуса в юном возрасте должна быть особая миссия, связанная с поддержанием ювентальности.
Удаление тимуса в детском возрасте приводит к преждевременному старению иммунной системы
Это вызывает изменения в Т-клетках, которые напоминают нормальное старение иммунной системы [3].
Без тимуса у взрослых увеличивается вероятность развития аутоиммунных заболеваний и рака. Очевидно, такое резкое повышение смертности от «всех видов болезней» связано с реализацией механизмов анизомалий* и повышением степени сенесцентности. Проще говоря, ослабевает Жизненная Сила на клеточном уровне, а количество сенесцентных клеток начинает доминировать над ювентальными.
Показано, что стареющая иммунная система не только допускает накопление сенесцентных клеток, но и сама способна «подталкивать» клетки к старению. Значит, тимус, как и эпифиз, — это еще один как анти-, так и просенесцентный регуляторный орган, а в целом это единая система регулировок сенилита и юности. Тимус чётко увядает с наступлением пубертата, гормональной зрелости. Но при подавлении его антисенесцентной функции запускаются механизмы сенесцента и во всех других тканях.
У евнухов может отсутствовать инволюция тимуса (атрофия) в связи с отсутствием половых гормонов.
Согласно этой гипотезе, в результате может увеличиваться продолжительность жизни евнухов. Так, исследование о придворных евнухах династии показало, что продолжительность жизни евнухов была на 15–20 лет больше, чем у мужчин с нормальной репродуктивной функцией, живущих в тех же условиях.
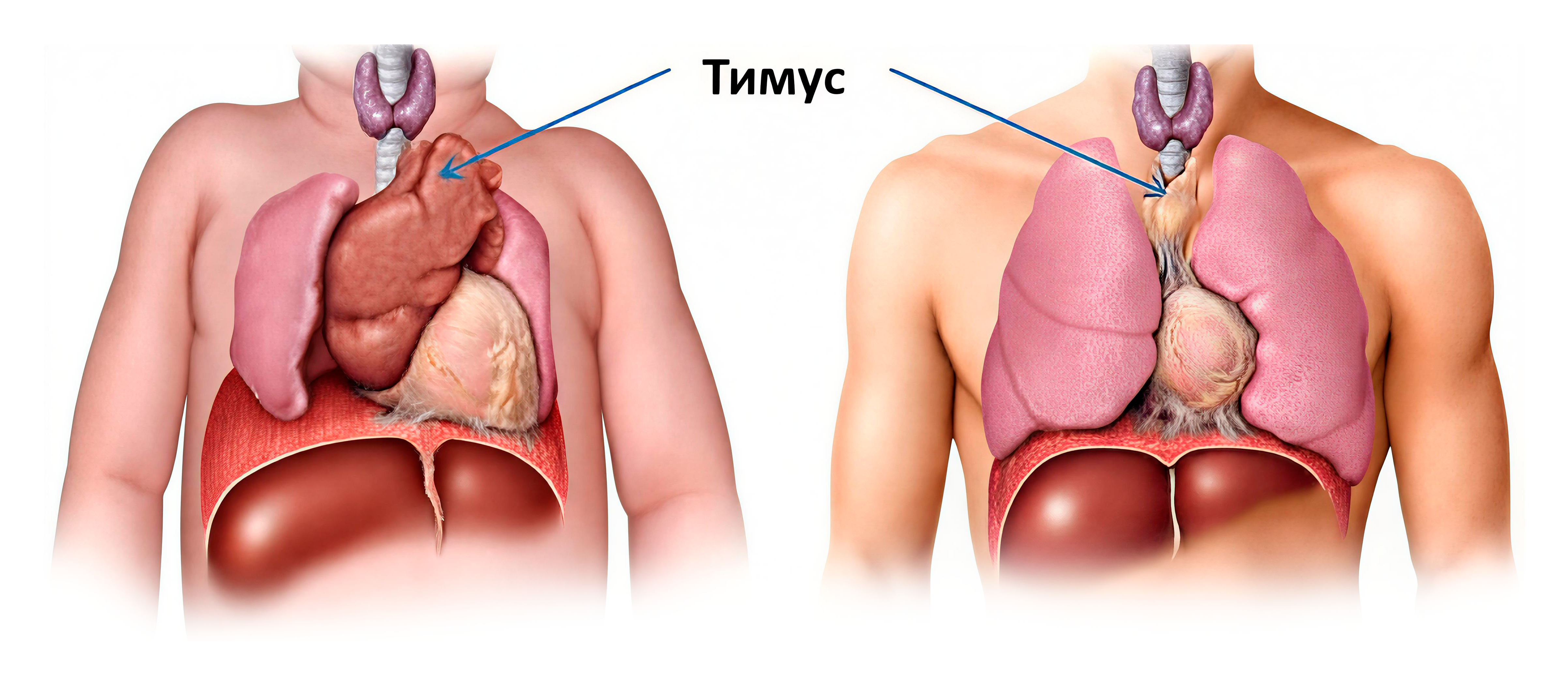
Рис. 1. На рисунке для сравнения приведены размеры тимуса у ребёнка (новорождённого) и у человека 50 лет. По размерам тимус соизмерим с другими важными органами, такими как печень, лёгкие и др. Эти огромные размеры явно показывают, что у тимуса, кроме иммунной функции, есть и другая — трофическая (иммунометаболическая), а точнее поддерживать ювентальность иммунных клеток. Наука пока об этом молчит и не догадывается
На рис. 1 показано, что у новорождённого ребёнка тимус имеет гигантские размеры, что указывает на его некую иную важную значимость не только в области иммунитета. Расцвет тимуса приходится на эмбриональный период. Это совпадает с периодом изобилия фетальных белков. Вырабатываются они в ювенильной печени и других органах, но не в тимусе.
Предназначение фетальных белков - защита плода от иммунного отторжения! Они делают иммунитет матери толерантным (терпимым) к антигенам. Но участвуют ли он в поддержании ювентальности клеток? Ясно, что омоложение матери не происходит (нет парабиогенного эффекта*).
Альфа-фетопротеин (AFP). Преобладающий сывороточный белок плода, который после рождения уступает место альбумину. AFP участвует в регуляции внутриклеточных механизмов роста и гибели клеток, а также снижает иммунологическую реактивность аллогенных лимфоцитов.
Таким образом, нельзя путать фетальные белки с UASP* – комплекс веществ, поддерживающих ювентальность* клеток и противодействующих SASP*.
Но есть сведения о некоторых белках (не AFP), которые играют важную роль в раннем эмбриональном развитии, например:
- Oct3/4. Белковый транскрипционный фактор семейства гомеобокс, который необходим для поддержания плюрипотентности стволовых клеток.
- Sox2. Белковый транскрипционный фактор семейства SOX, который связывается с малой бороздкой ДНК и также играет решающую роль в раннем эмбриональном развитии и самоподдержании популяции клеток.
Очевидно ювентальность является результатом изначальной внутренней настройки популяций всех иммунных клеток на ювентальность (см. ниже кейлонную* гипотезу системы саморегуляции популяций клеток).
Автор предлагает выделить такие девственные модификаты ювентального типа и обозначить как Mu, чтобы затем различать их от модификатов сенесцентных, и обозначить как Мs. Очевидно, через некие кейлонные белки и UASP эти иммунные девственные клетки «регулируют» все остальные иммунные клетки-резиденты данной ткани, а те в свою очередь влияют на активность или подавление стволовых клеток каждой ткани. Это аналогично тому как сенесцентные клетки «заражают» своим белком другие клетки. Они содержат белок ReHMGB1. Молекула начинает воздействовать на рецепторы соседних клеток, и те, в свою очередь, тоже «заражаются» процессом старения. Итак, есть белки ювентальности, а есть белки сенесцентности?
Но как клетки Mu узнают, что надо перейти в Ms если для этого нет внешнего сигналилинга? Регулировка таких тканей происходит сугубо изнутри согласно принципам существования клеточных популяций на основе саморегуляции и самоограничения роста. Морфогенез и саморегуляция ткани в целом основаны на этих же принципах, являющейся по сути ансамблем различных популяций с учетом взаимосаморегулировки в ней всех клеточных популяций. Каждая популяция, будучи автономной, в тоже время соподчинена требованиям ткани. Каждый орган состоит в свою очередь из ансамбля тканей, тоже существующих на правилах саморегулировки.
Кейлонная концепция системы саморегуляции даёт объяснение тканевым гомеостазам [4]. В этом случае ткань изнутри знает до каких размеров ей расти и сколько циклов клеточного деления надо пройти, а также знает (коммитирована) когда надо остановить рост и запустить механизмы сенесцента. В данном случае сенесцент является механизмом через которые реализуются эти регулировки.
Это означает что сенесцент может запускаться как сверху, так и исходить снизу по правилам кейлонной саморегулировки гомеостазов ткани. Кейлоны это вещества и гены, регулирующие рост ткани.
Очевидно, известный лимит Хейфлика (ограниченного числа репликаций клеток до 52) тоже связан с этими кейлонными саморегулировками. Клетки в культуре ткани это тоже самое, что вырванный из контекста текст, работают на принципах культур самоограниченных по размеру и числу репликаций. Таких коммитаций или самоограничений в растительном мире нет. Но те же клетки в составе ткани и организма могут работать уже по другим правилам.
Инволюция тимуса – проявление программы старения или программы развития? Автор позиционирует ювенильный тимус как орган поддержки ювентальности иммунных клеток и среды крови. Детский тимус максимально способен к парабиогенезу, то есть обеспечивает мощную доминантность ювентальности над сенесцентом. Очевидно, вытяжки ювенильного тимуса будут противодействовать лимиту Хейфлика, когда клетки in vitro способны к репликациям около 52 раз.
Ряд данных свидетельствуют, что эпифиз является органом иммунной системы, а верифицированные в нём иммунные клетки могут выполнять компенсаторную роль при возрастной атрофии тимуса [5]. Но, с другой стороны, известно, что мелатонин способен активировать вилочковую железу (тимус) и стимулировать иммунитет. С угасанием эпифиза угасает и тимус. Обращает на себя внимание, что тимус, как и эпифиз, угасает в юности и даже детстве. В обоих этих органах происходит инволюция, вырождение. Расцвет юности возможен только в условиях максимальной активности эпифиза и тимуса.
Для внутренних процессов человеческого организма характерны совершенно иные темпы изменений. «Возрастной порог» нашей иммунной системы расположен гораздо ближе к детству, чем к старости. Уже с первого года жизни в тимусе ребёнка начинают происходить драматические изменения: функциональная ткань органа заменяется на соединительную, уменьшаясь каждый год на 3 % до 35–45 лет, а после 45 — на 1 %. В 70 лет соединительная ткань занимает 90 % тимуса [6]. Наиболее активно тимус функционирует в пренатальный период и до наступления половой зрелости.
Автор выдвигает концепт, что это связано с тем, что тимус в юности, кроме иммунных функций, также вместе с высоким уровнем мелатонина ещё поддерживает определённый статус ювентальности иммунных клеток. И в этом ему помогает мелатонин эпифиза. Это означает, что эпифиз и тимус — это составные единой системы, у которых имеется, кроме других функций, одна общая сторона взаимодействия — поддерживать ювенил и ювентал.
Кроме поддержки ювентальности, тимус противодействует онкологическим процессам. Дело в том, что сенесцент и онкология имеют много общих механизмов. Автор считает, что возрастная онкология — это одно из проявлений сенесцента. Оказывается, тимус участвует в защите организма человека и от рака. Показано, что тимус имеет решающее значение для здоровья взрослых в целом, а также для предотвращения рака и, возможно, аутоиммунных заболеваний.
При этом эпифиз поддерживает на общеорганизменном уровне и противостоит сенилиту за счёт ювенила, тогда как тимус работает на клеточном уровне иммунитета и противостоит сенесценту за счёт ювентала.
Люди с прогерией (преждевременное старение) живут намного меньше. Также показано, что прогерия связана с изменениями в тимусе, при этом заболевании наблюдается инволюция тимуса (уменьшение его размеров)! Это важнейший аргумент того, что сенесцент и сенилит начинаются с тимуса. Продолжительность их жизни колеблется от 7 до 28 лет, в среднем составляя 12–13,5 года [7]. Основные причины летальных исходов — острый инфаркт миокарда, застойная сердечная недостаточность, инсульты на почве атеросклероза — типичные преждевременные анизомалии.
Но это же означает и обратное: чем дольше сохраняется юность тимуса, тем дольше организм не стареет. Согласно мнению многих учёных, сохранение функции тимуса может продлевать молодость организма. Темпы старения сопряжены с тимусом и иммунной системой.
Также выявлено, что в зависимости от возраста наступления первой менструации у девочек зависит проявление скорости наступления болезней возраста (анизомалий). Этот момент (возраст запуска менархе) может быть настоящей «лакмусовой бумажкой» её будущего здоровья. Женщины, у которых менархе (первая менструация) случилось до 10 лет, в зрелом возрасте гораздо чаще страдали от ожирения, гипертонии, диабета, сердечно-сосудистых заболеваний и осложнений во время беременности (например, преэклампсии). Все эти возрастные проблемы одновременно являются не только гормонозависимыми, но и иммунозависимыми. А вот тем, у кого первая менструация началась позже 15 лет, повезло чуть больше с весом — риск ожирения у них был ниже. Но! Увеличивалась вероятность нерегулярного менструального цикла. Очевидно, что раннее менархе связано с ускоренным старением тимуса и эпифиза, а значит, и ускоренным старением всего организма. Неотенические типы живут дольше. Ускорение старения эпифиза усиливает элевацию гипоталамуса.
Идеальное Здоровье – это не только крепкий иммунитет, но и гормезис, которые возможны только в молодости, юности.
Самый высокий пик показателей Витаукта и Жизненной Силы — в период становления пубертата. Именно в этом возрасте самая мощная поддержка от врождённого и приобретённого иммунитета, которые и «открывают дверь» в сторону иммуноювентализации или к иммуностарения. Приобретённый иммунитет – это по сути клонотипический иммунитет (резистентность – нечувствительность), ответственный за "иммуносенсибилизацию" (иммуносенесценция) — процесс ослабления иммунитета, который возникает с возрастом на ряд специфических и неспецифических факторов экзогенной природы. Это проявляется в уменьшении производства новых лимфоцитов в костном мозге и тимусе, а также в снижении способности иммунных клеток распознавать и уничтожать возбудителей. Но таковыми могут стать и факторы эндогенного характера, сопряженные с сенесцентом и иммуностарением. Среди них эпигенез и онтогенез, исключающие ювентальность клеток и ослабляющих их Жизненную Силу.
Как итог резкое повышение заболеваемости и смертности. Причины смерти у пожилых людей чаще, чем у людей в возрасте от 25 до 44 лет: рак — в 43 раза чаще, пневмония и грипп — в 89 раз чаще, болезни сердца — в 92 раза чаще, а инсульт и хронические заболевания лёгких — более чем в 100 раз чаще!
Механизм иммуносенесценции:
- Сокращение количества наивных Т-лимфоцитов — накопление клеток памяти не компенсирует эту утрату, снижая адаптацию к новым патогенам.
- Накопление миелоидных клеток-супрессоров и позднедифференцированных Т-клеток.
- Снижение цитотоксической активности иммунных клеток, а также экспрессии функциональных молекул, связанных с цитотоксической активностью (гамма-интерферон, гранзим B и перфорин).
- Изменение метаболизма иммунной системы: повышенный гликолиз и выработка активных форм кислорода, снижение синтеза митохондрий.
Причины: сенесцент и сенилит.
Возраст – это всегда высокая активность зрелого гипоталамуса, который находится в противофазе с ювентальностью тимуса и ювенильностью эпифиза. Зрелый гипоталамус всегда будет их подавлять и доминировать над ними. Следовательно, высокая ювентализирующая активность тимуса и ювенилизирующая эпифиза возможны только в возрасте юности, до пубертата. Поддержание максимального здоровья и долголетия на фоне сохранения зрелости организма невозможно.
Эпифиз — основа Витаукта в юности, а тимус — база Жизненной Силы, то есть ювентальности клеточного уровня. Максимальный накал Витаукта и Жизненной Силы — это допубертатный период, то есть ранняя юность (но не детство). Также они интегрированы на гормезис и гомеостазы. Следовательно, максимальное проявление Витаукта и продление жизни возможно только на этапе ювенил. Это означает, что высочайшая мощь Витаукта для продления жизни возможна только при поддержании статуса неотении*. Только здесь возможно обеспечить высшую эффективность здоровья. Кстати, неотения не означает отсутствие репродуктивных способностей и инфантильность. Аксолотли, сохраняющие неотению, тем не менее легко размножаются.
Все эти процессы с возрастом движутся, изменяются посредством механизмов гормезисорезов* и гомеостазорезов*. Все остальные этапы после юности — это неизбежное отодвижение, удаление от здоровья, то есть выход из зоны оптимума как для Витаукта, так и для Жизненной Силы. Чем слабее Жизненная Сила (ювентальность), тем слабее Витаукт (ювенильность), и наоборот: чем слабее Витаукт, тем слабее Жизненная Сила. Витаукт — это сугубо прерогатива юности. Крайними антиподами для них являются сенесцент и сенилит.
Первично процесс старения начинается на уровне Жизненной Силы, то есть посредством сенесцента. Начинается этот процесс в юности и пубертате, когда угасают-подавляются тимус, а затем эпифиз. Вместе с этим ослабевает и их миссия по ограничению гиперфункции и перепрограммирования иммунных клеток. В крови появляются SASP*, которые приобретают решающую значимость вместо UASP*, а также «зрелые» иммунные клетки, которые перепрограммированы и отличаются от тех, что были до пубертата. Это происходит в связи с изменением гормонального профиля, в частности на фоне усиления половых гормонов и снижения уровня гормонов роста. Мощь Витаукта резко возрастает, но без обеспечительной поддержки со стороны Жизненной Силы. Усиление основной мощи Витаукта перераспределяется в репродуктивном направлении.
Витаукт в это время находится в расцвете, апогее, и он еще долго будет поддерживать организм, вплоть до зрелости и адальтуса*. Но при этом происходит перекос — доминирование Витаукта над Жизненной Силой. Потребности отстают от возможностей. Но долго такое доминирование существовать не может. Разрыв в балансах этих процессов ведёт к истощению Витаукта, ослаблению его возможностей. Такие ограничения, в свою очередь, ведут к ослаблению потенциала поддержки для Жизненной Силы, он тоже слабеет за счёт перекоса между SASP и UASP, нарастания процессов онтофизиса* и эпигенеза. Идёт медленное уменьшение потенциалов то Витаукта, то Жизненной Силы. Эта раскачка идёт волнами, ступенчато, пока организм не пройдет весь свод разных периодов, этапов-ступеней на онтодианной линии. Именно это взаимоослабление одного уровня другим является драйвером онтогенеза, ведущего к геронтосу и мортусу. Это когда становится невозможной поддержка Витаукта для Жизненной Силы и наоборот.
Эпифиз реализует свои задачи по продвижению по онтодианной линии (созревание организма на верхнем и нижнем уровнях в сторону от ювенила, пубертата к адальтусу… сенилиту) посредством настройки тимуса. Но тимус своей активностью тоже модулирует эпифизарный иммунный камертон. Запустить сенесцент микроглии эпифиза могут сигналы со стороны тимуса.
Тимус — один из первых органов, где начинают регистрироваться возрастные изменения негативного характера. С возрастом масса тимуса уменьшается, его корковый слой замещается соединительной тканью. Максимальный уровень выработки гормонов тимуса наблюдается в раннем возрасте — до начала полового созревания.
Выявлены вещества, такие как BMP4 и активин, которые являются факторами роста и дифференцировки, ключевыми в самообновлении и дифференцировке эпителиальных стволовых клеток тимуса, и изменение их уровней в результате старения вызывает потерю этих эпителиальных клеток. Эта потеря в результате приводит к снижению производства Т-клеток в тимусе, что в конечном итоге оставляет нас открытыми инфекции и болезням. Это исследование является первым в мире и выявляет основную причину, по которой мы испытываем потерю эпителиальных стволовых клеток тимуса, а также молекул и механизмов, которые управляют этим процессом.
Иммуносенесценция - конечным результатом этого процесса является то, что наше тело больше не может обеспечить эффективную защиту от болезней, неправильно активируется, что приводит к иммунной дисфункции и хроническому воспалению. Уменьшение тимуса связано с риском развития рака, который резко возрастает с возрастом, согласно концепции иммуносенесцентного рака. Иммунное старение также сильно коррелирует со множественными возрастными патологиями.
Эпифиз тоже претерпевает возрастные изменения: угасание эпифиза начинается после наступления пубертата. Это указывает на то, что эпифиз подчиняется сигналам тимуса на сенесцент. У пожилых людей наблюдается атрофия паренхимы эпифиза, в которой локализованы мелатонинсинтезирующие пинеалоциты. При этом у 29 % пожилых людей функциональная активность эпифиза не снижается, и высокий уровень секреции мелатонина может способствовать восстановлению функций тимуса даже при значительных инволютивных изменениях. Эти данные указывают на то, что можно целенаправленно давать длительно (6 и более месяцев) взрослому человеку высокие дозы мелатонина (25 мг/сутки), что поможет восстановить и поддержать высокий уровень работы тимуса, что, в свою очередь, со временем само приведёт к активации эпифиза. Активность эпифиза сдерживает половую зрелость, а затем и сенилит… Через механизмы обратной связи это продлит юность тимуса.
На первом этапе жизни эпифиз и тимус работают как синергисты, но после пубертата* (половой зрелости) переходят на путь антагонизма. На втором этапе жизни тимус тоже оказывает своё влияние на эпифиз, но уже обратным путём, то есть посредством усиления сенесцента в нём. Это связано с тем, что между ними появляется мощный посредник (триггер) — репродуктивное созревание и смена гормонального профиля. Половые гормоны подавляют как тимус и его ювентализирующую активность, так и эпифиз и его ювенилизирующую активность.
Если это так, то сохранение высокого уровня мелатонина, возможно, сможет вернуть к работе тимус, а значит, поддерживать юность иммунных клеток. Только юные иммунные клетки способны удерживать ювентальность своих сородичей-резидентов. Через них обеспечивается ювенальная трофика тканей, которая всегда идеальна по сравнению с трофикой тканей в других возрастах. Это обеспечивается благодаря иммунометаболической функции ювентальных клеток. Тогда как сенесцентные клетки настроены на метавоспаление* — это форма хронического воспаления, вызванного хроническим метаболическим дисбалансом, например, в связи с входом сенесцентных клеток в режим неоптимальных гомеостазов или гликолиза. При этом:
- концентрация медиаторов воспаления низкая, процесс вялотекущий, малозаметный;
- поддерживается иммунной системой, течение воспаления длительное, само не проходит.
Омоложение тимуса, или Перспективы отключения старения
Тимус выполняет не только ключевые функции в иммунной системе, но и, по последним научным открытиям, имеет удивительный потенциал в управлении ходом биологических часов и, возможно, в выключении старения. Ряд специалистов согласны с тем, что вилочковая железа воздействует на биологические часы нашего организма. Автор также считает, что его роль — не просто участие в поддержке (сохранении) клеточного ювентала*, а значит, отодвижении геронтоса, но и в обновлении или ювентализации иммунных клеток, что создаёт условия для замедления процессов старения и управления биологическим возрастом.
Воздействие на вилочковую железу может замедлить процессы старения и продлить здоровую продолжительность жизни.
Старение тимуса ведёт к сенесценту в первую очередь среди иммунных клеток, в т. ч. макрофагов-резидентов, а через них ко всему спектру анизомалий. Сенесцент — это нижний этаж геронтоса, где верхним этажом является сенилит. Поэтому бороться с геронтосом невозможно, если действовать только на один из этажей, например, на верхний через эпифиз (сенилит) или нижний этаж через тимус (сенесцент). Это взаимозависимые звенья единого кольца. Система имеет одновременную автонастройку друг на друга как сверху, так и снизу. Эпифиз не может быть ювенильным без ювентальности тимуса, а тимус не может сохранять ювентальность без ювенила эпифиза.
Удаление эпифиза может влиять на работу тимуса. Установлено, что удаление эпифиза или его функциональное выключение приводит к ограничению иммунной реактивности со снижением гуморального и клеточного иммунитета [8].
Удаление тимуса стимулирует половое созревание. Тимус и половые гормоны влияют друг на друга. Половые гормоны угнетают тимус.
Удаление гонад в детстве снижает темп инволюции тимуса. Быстрое и интенсивное развитие половых органов всегда говорит о снижении функции эпифиза и прекращении его доминирования над гипоталамусом [9].
Тимус в юности значительно повышает выработку мелатонина – активирует эпифиз.
Угасание эпифиза – путь к разблокированию зрелости гипоталамуса. Это означает, что ослабление ювентальной (поддержание клеточной молодости) функции тимуса приводит к ослаблению ювенильной функции эпифиза (сохранение гормонального статуса сдерживающего половую зрелость гипоталамуса). Молодой тимус поддерживает юность эпифиза. Удаление юного тимуса (в детстве) — это утрата потенциала ювентализации, путь к сенесценту и ускоренному сенилиту иммунной системы, а через неё стареет и весь организм.
Мелатонин подавляет возрастную инволюцию тимуса. Мелатонин способен увеличивать клеточность тимуса, усиливая пролиферацию клеток.
Таким образом показано что в молодом возрасте имеется прямое и обратное реципрокное действие тимуса и эпифиза друг на друга. При старении характер связи между этими железами нарушается, что является проявлением возрастной дисфункции иммунной системы.
Известно, что у мышей, которые рождаются без тимуса, наблюдается задержка развития, а также подверженность раннему старению. Также у них стимулируется процесс канцерогенеза. Что означает подверженность раннему старению? По концепции автора юный тимус определяет юность иммунных макрофагов резидентов, которые вырабатывают свой UASP* и тем самым противодействуют сенесценту иммунных и рабочих клеток человека почти до 12 лет; если тимуса нет, то все остальные иммунные клетки быстро переходят на сенесцент, но в данном случае говорится о подверженности раннему старению, а не о быстром старении. Теоретически противодействие раннему старению означает устранение хронического провоспаления, оксидативному стрессу и всему комплексу проявлений сенесцента. Следовательно, роль иммунных клеток в этом направлении связана с недопуском к провоспалениям и оксидативному стрессу, гашению таких пожаров. Но если такого иммунитета нет, то такие тлеющие «пожары» быстрее выжгут организм и быстрее приведут к старению. Отсутствие тимуса может сказаться и на плохой защите организма от внешних патогенов, что тоже ускорит старение.
Кстати, Куркумин может сдерживать сенесцент (см. рис. 2).
 КУРКУМИН-АДВАНС
КУРКУМИН-АДВАНС
Рис. 2. Для сдерживания пожара хронического сенесцентного провоспаления, защищает тимус от старения. Геропротектор. Антиоксидант – стимулирует активность антиоксидантных ферментов. Модуляция белков, связанных со старением, подавляет экспрессию белков, которые усиливают старение, например mTOR, воздействует на теломеры, усиливая теломеразу. Противодействует провоспалению. Влияет на апоптоз и аутофагию. Защита нейронов
Считают, что иммунный статус детей после неонатальной тимэктомии аналогичен результатам старения иммунной системы у пожилых людей после инволюции тимуса. Удаление старого тимуса не влияет ни на старение, ни на омоложение, но увеличивает смертность от ряда заболеваний и онкологии. Таким образом, тимус ↔ эпифиз – это первичная ось, где регулируется длительность этапа юности и через которую можно влиять на неотению – продлевать юность.
Тимус в роли эмитента* указаний-регламента развития. Тимус можно условно (после его иммунных обязанностей) также назвать и органом эмитентом (банком), то есть раздающим важную информацию предписаний (указания-«ценные облигации-дотации» для реализации), то есть направления того или иного пути развития (юность–зрелость), тогда как эпифиз является для него первым органом-эмиссаром, который воспринимает эти указания и их диверсифицирует (преобразует, переводит на другой язык) для дальнейшего осуществления. Тимус здесь фактически играет роль прибора навигатора-гироскопа, определяющего степень готовности и сроки для «сброса тормозов» в эпифизе. Иммунные клетки-резиденты (макрофаги-нейроглия) эпифиза обладают чувствительностью, готовностью к этому. Остаётся неразгаданным как тимус определяет эту степень готовности к переключениям, перехода на новый режим работы, откуда поступают сигналы? Относительно какого гормонального параметра он ориентируется? Известно, что сигналы юного эпифиза блокируют гипоталамус. Позже ювенилизирующий функционал эпифиза снижается в 10 раз.
Автор выдвинул иммунную концепцию созревания оси тимус-эпифиз-гипоталамус. Это означает, что диверсификация осуществляется в первую очередь через иммунную систему эпифиза (она составляет 40% от его объёма), она же приёмник иммунных сигналов (иммунные клетки-резиденты) и запускает в нём программу на локальное (in situ) отключение через сенесцент (модификацию, отключение функционала в рабочих стем-клетках), что ведёт к подавлению в нём высокого уровня виргинальной (девственно-детской) активности (производство мелатонина и др.). Сигнал на диверсификацию поступает через вещества подобные CD1 (кластер дифференцировки-1), а точнее через вещества провоспаления, цитокины, которые вырабатываются в иммунных Т-хелперных клетках (типа CD4+ клетки?), и другие предписывающие из этой же группы. Молекула CD1 играет роль в иммунной системе. Она связывает непептидные антигены и представляет их подмножествам T-клеток со специализированными функциями. Это семейство трансмембранных гликопротеинов. Таким образом, это начало для подавления этапа ювенильности = ювентоса, который был связан с высоким уровнем мелатонина, что реципрокно затем сказывается на перестройках в гипоталамусе и переключению его активности на половую зрелость. Следовательно, изначальный приказ на созревание гипоталамуса отдаётся в тимусе.
Как вывод: контроль и запуск перехода организма на новый этап онтогенеза осуществляется через иммунную систему путём локального сенесцента (в иммунных его клетках) в эпифизе, а затем сигнал открывает дорогу для новых дифференциаций и созревания в ряде центров в гипоталамусе.
Вопрос: возможно ли через реювенилизацию тимуса вернуть юность в эпифиз и гипоталамус? Но для этого надо было бы вернуть ювенильный статус иммунных-резидентов эпифиза, которые просенесцентировали и атрофировались. Начинать надо было бы с возрождения их. Но с другой стороны омоложение тимуса возможно только на фоне омоложения эпифиза. Так может тогда правильнее начать с омоложения эпифиза, а он создаст условия для запуска процессов омоложения в тимусе? Но функционал эпифиза зависит от статуса его иммунной стороны, обеспечивающей его трофику и поддержку. Без поддержки тимусом иммунной ювентальности эпифиза он не может быть высоко активным. А без активности и юности эпифиза тимус не может сохранять ювентальность.
В то же время, ряд данных указывает, что даже через постаревший эпифиз можно омолаживать тимус, а для этого достаточно обеспечить компенсацию его возрастной недостаточности путём введения извне нужных доз его функциональных веществ, как Мелатонин + Эпиталон + Куркумин-Адванс + Лютеолин и др. Возможно это частично позволит перемодифицировать старые иммунные клетки в молодые. Ожидается, что это позволит прийти к обратному омоложению эпифиза со стороны омоложенного тимуса. Вопрос открытый… Известно лишь, что тимус и эпифиз «закольцованы» так, что теоретически омоложение эпифиза позволяет омолодить и тимус. В свою очередь омоложение тимуса позволяет омоложению эпифиза. Та сторона этого замкнутого круга, которая стареет первой, то есть инициирует процесс старения системы, и является драйвером старения всей системы. Кто из них ведущий, а кто ведомый? Для получения омолаживающего сигнала со стороны молодого эпифиза его сила влияния должна быть выше.
Что такое реципрокная регулировка? Итак, между этими органами, закольцованными в единую систему, существует функциональная обратная связь, которая работает реципрокно, пошагово, так как вещества вырабатываемые эпифизом, способны в свою очередь замедлять инволюцию тимуса, в том числе и восстанавливать его функции. Реципрокно означает, что тимус раскачивает эпифиз и при достижение определённой амплитуда эпифиз запускает обратный сигнал для раскачки тимуса (сигнала противодействующего его инволюции). Таким образом, происходит прямой и обратный сигналы. Каждый сигнал действует не моментально на сигнал, а при раскачке, достижении определённой амплитуды, что и является размером шага и началом шагового ответа. На регистрацию каждого шага в противоположном рычаге единой системы уходит достаточно много времени, чтобы в обратной стороне маятника накопить усилия для противодействия…
Роль триггерных факторов корректировки маятниковой авторегулировки оси тимус-эпифиз. Но в эту маятниковую регулировку постепенно вмешиваются триггерные факторы корректировки. Если бы не было триггерных факторов, то такая система могла бы работать безлимитно. Не является ли эта концепция подтверждением случая неотении с Денисом Вашуриным [19], у которого из-за гипофизарного нанизма (недоразвитости) осталась недостаточной выработка гормона роста, что и стало причиной исключения из этой системы триггерного фактора, который и выводил систему из непрерывного баланса.
Но в данном случае тогда следовало бы сделать вывод, что гормон роста в высоких уровнях поддерживает на начальных этапах ось тимус-эпифиз, но при снижении его уровня почти в два раза к возрасту 12 лет он перестаёт поддерживать незрелость этой оси (см. рис. 3).
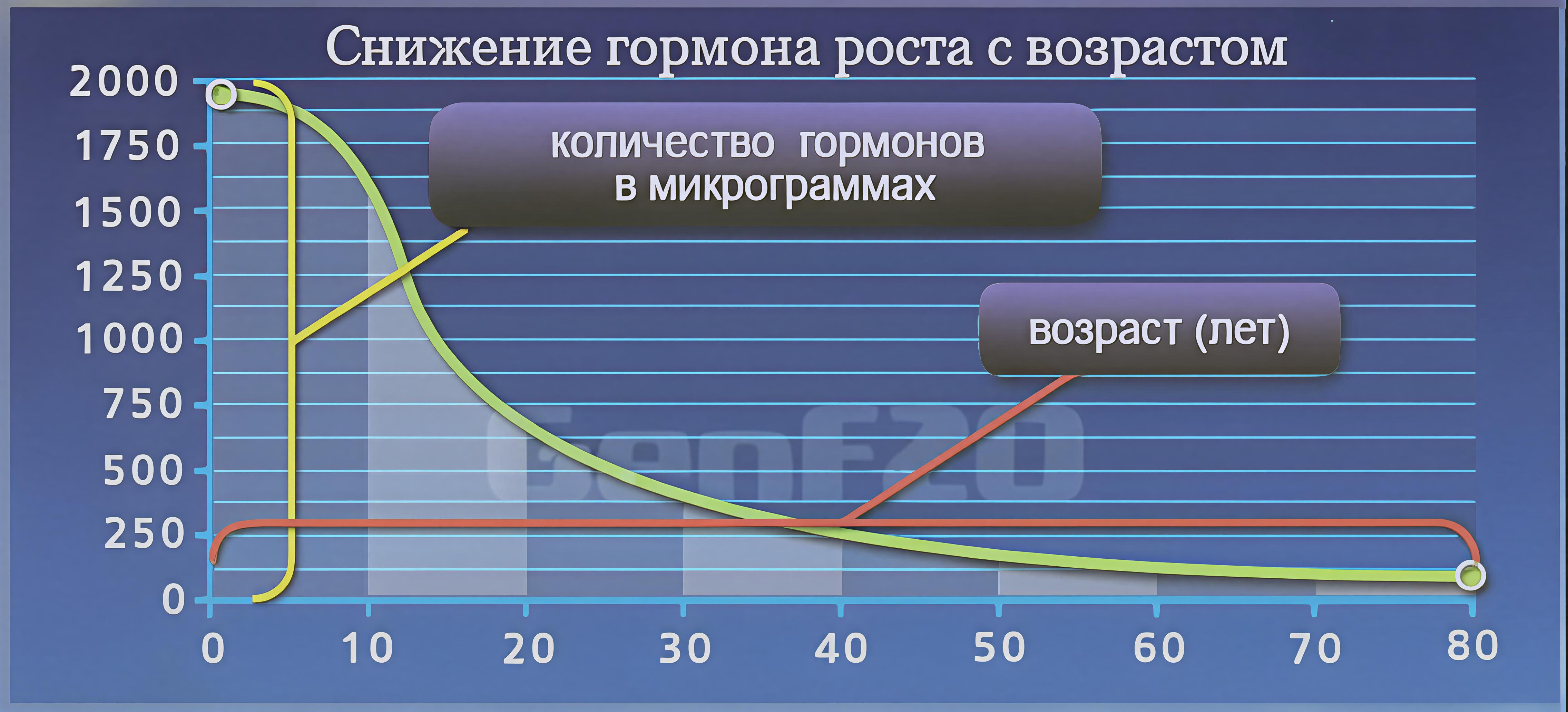
Рис. 3. На рисунке показана динамика уровня гормона с возрастом, из которой видно что при рождении этот уровень максимален, к возрасту 12 лет снижается в 2 раза, а к 30 годам идёт резкое снижение его выработки и приближение к минимальному уровню. Высокие уровни гормона роста совпадают с периодом высокой активности оси тимус-эпифиз.
Но случай неотении с Денисом Вашуриным противоречит предлагаемой концепции, так как у этого человека изначально был снижен уровень гормона роста, однако это не повлияло на ось тимус-эпифиз и она сохраняла ювенильность.
Очевидно эта ось зависит не от СТГ, а от ИФР (инсулиноподобного фактора роста). Есть целый ряд данных показывающих его связь со старением (см. рис. 4).
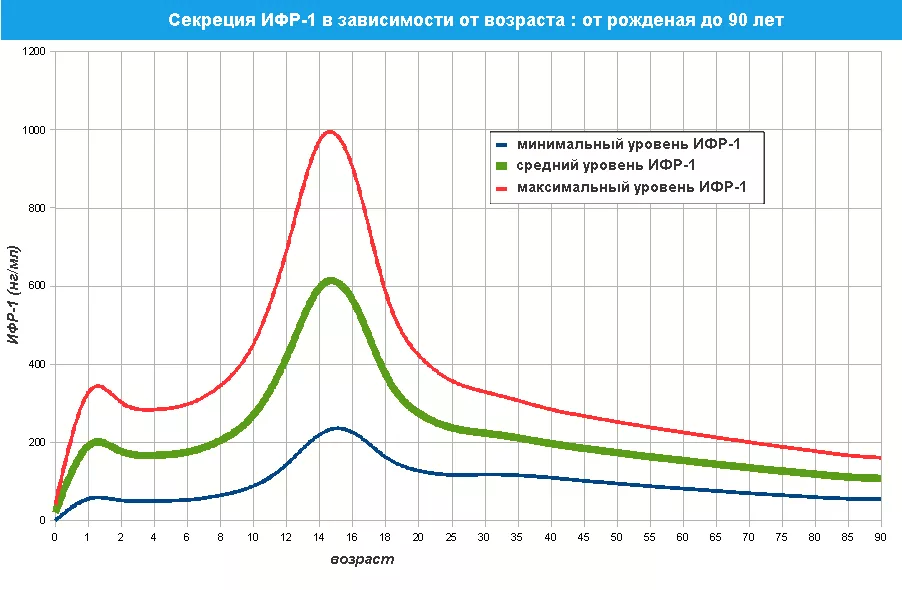
Рис. 4. На рисунке показана динамика изменений уровня ИФР в зависимости от возраста. Видно что максимальный уровень этого фактора достигает в 15 лет, а затем он значительно снижается.
Сам по себе СТГ на рост не влияет. Гормон роста, попадая в кровь, стимулирует выработку Инсулиноподобного фактора роста (ИФР), в основном в печени. ИФР (IGF-I, IGF-II), играют ключевую роль в пролиферации и дифференцировке специфических функций многих типов клеток. Так может именно ИФР влияет ось тимус-эпифиз? Тогда это означает что в случае с Вашуриным был сбой в этом факторе? Очевидно к этому фактору была утрачена чувствительность. Тем не менее, известно что люди карлики с врождённым дефицитом СТГ живут меньше чем нормальные. Также известно, что аномально высокие уровни СТГ и акромегалия укорачивают жизнь. Мало СТГ – плохо, много СТГ тоже плохо. Искусственное добавление СТГ с возрастом повышает разные риски. В тоже время было показано, что снижение активности оси СТГ/ИФР-1 продлевает продолжительность жизни. Ограничение калорийности, которое является одним из наиболее действенным способов увеличения продолжительности жизни, также снижает активность оси СТГ и ИФР. Животные, которым вводили СТГ, проявляли снижение продолжительности жизни 30-40%. Мыши лишенные гормона роста имеют значительное снижение продолжительности жизни. Но это противоречит данным о снижении продолжительности жизни у людей карликов.
Замечу, что снижение потребления белка уменьшает уровень ИФР-1 на 25 %, что может быть важной частью «противораковых и антивозрастных диетологических вмешательств». Но очевидно в данном случае недостаток ИФР вызвал угнетение усвоения белков клетками на 25%, а это не позволило сработать механизмам «созревания» в клетках тимуса или эпифиза, то есть остановилось преобразование иммунных клеток в новые модификаты. Их клетки не смогли перейти некий рубеж, нужный для запуска кейлонных программ или образования модификатов.
На первый взгляд система замкнута и может поддерживать сама в себе неограниченно постоянство, гомеостаз. Тогда следует объяснить почему происходит односторонний сдвиг в сторону сенесцента тимуса, а затем эпифиза, если они закольцованы и каждая из сторон должна автоматически компенсировать эти сдвиги, возвращать в исходное состояние противоположное крыло?
В тоже время возникает вопрос, почему вещества эпифиза могут омолаживать тимус? Ведь из выше сказанного следует, что тимус заставляет эпифиз стареть, а не наоборот. Но это происходит на определённом продвинутом этапе, но не в детстве, когда тимус действует омолаживающе. То есть тимус сначала сам меняет перестраивает себя, а потом уже влияет и на таргет. Эпифиз при этом (в юности и детстве) наоборот заставляет тимус поддерживать омоложение, омолаживаться, не давать ему выйти на режим старения, то есть противодействует этому. Очевидно, идёт взаиморегуляция между ними, которая должна была бы поддерживать равновесие, паритет между ними, но если паритет смещен, то начинает работать принцип доминирования. Как происходит смещение паритета? Это возможно когда в эти взаимоотношения вмешивается третье звено, играющего роль триггера – стороннего рычага регулировки. Этот триггер односторонне влияет на один из рычагов маятниковой системы: какое крыло сильнее – то и задаёт тон.
Роль соматотропного гормона роста (СТГ) в возрастной коррекции оси тимус-эпифиз?
Известно, что на первых этапах онтогенеза организма уровень СТГ, его выработка и концентрация в крови максимальны, а после 12 лет снижаются. Вырабатывается он в гипофизе. Не является ли снижение уровня СТГ стартером = триггером для модификаций в тимусе (Mu на Ms – ювенильных на сенесцентные)? Но глобальная инволюция тимуса начинается в раннем детстве, а уровень СТГ снижается после 12 лет. В этом же возрасте начинается инволюция эпифиза. Так может СТГ действует на прямую на иммунную систему эпифиза? Ясно что с 12 летнего возраста снимается полностью блокирующая половую зрелость триада тимус-эпифиз-СТГ. Тимус реагирует не только на гормоны эпифиза, но и на уровень СТГ. Действительно СТГ влияет на тимус, участвуя в развитии и функционировании этого органа. Рецепторы СТГ идентифицированы на поверхности клеток иммунной системы, в том числе на тимоцитах.
Механизм воздействия:
СТГ регулирует тимическое микроокружение, влияя на различные процессы в тимусе:
- Стимулирует пролиферацию тимоцитов. Гормон ускоряет включение ЗН-тимидина в ДНК кортизончувствительной популяции тимоцитов.
- Повышает секрецию и высвобождение цитокинов (прежде всего, провоспалительных интерлейкина-1 и интерлейкина-6), хемокинов и тимулина. Их предназначение активировать, повышать готовность к борьбе. Но к 10-12 годам уровень СТГ резко снижается.
Но если стресса нет, а уровень СТГ растёт, то это усилит провоспалительный фон, что не благоприятно сказывается на воспринимающем иммунитете эпифиза, что и подавит его работу. Это означает, что подавление эпифиза идёт через неспецифическую сторону провоспаления, через сенесцент, а проще говоря через механизмы стресса и угнетения. Причём стресс идёт не напрямую, а через не стрессовые механизмы провоспаления. Стресса нет, а провоспаление есть. Это скрытый или ложный эустресс (положительный = регуляторный стресс), на который эпифиз имеет повышенную чувствительность.
- Увеличивает выработку белков внеклеточного матрикса.
- Увеличивает отложение белков, способствующих миграции клеток, таких как ламины и стромальный клеточный фактор-1.
- Подавляет апоптоз тимоцитов – например, апоптоз, вызванный глюкокортикоидами.
Также СТГ вызывает качественные и количественные изменения в структурах тимуса: увеличивает численность популяции тучных клеток, способствует созреванию в них гепараина и увеличению доли дегранулированных форм.
Таким образом, СТГ становится триггером, третьим звеном во взаимоотношениях тимуса и эпифиза, что и определяет реципрокную их регулировку, то есть не бурные трансформации, перестройки, а медленные пошаговые.
Между эпифизом и тимусом существует принцип маятника и доминирования. На определённом этапе силы тимуса и гипоталамуса начинают доминировать и чаша маятника начинает перевешивать в сторону активности, зрелости гипоталамуса, но при этом угнетается эпифиз.
Кстати, с возрастом (к 30 годам) и созреванием гипоталамуса, уровень выработки СТГ снижается.
В свою очередь СТГ находится в антагонистических отношениях с гормонами половой зрелости, то есть снижение уровня СТГ ведёт к росту половых гормонов. СТГ действует не напрямую, а опосредовано через инсулиноподобные факторы роста (ИФР).
Модификации сенесцента или ювентальности клеткам задаёт тимус или иммунные клетки. Эти модификации осуществляются с помощью веществ из группы типа CD1. Такой вывод вытекает из приведённых выше посылок. При такой виргинальной ювентальности клеток не происходит укорочение теломер, что означает непрерывное сохранение удлиненных теломер — концевых участков хромосом, защищающих ДНК от повреждений при делении клетки и обеспечивающих возможность к нормальным делениям, что невозможно при сенесценте. Значит нет и клеточного сенесцента. Тот сенесцент, который известен в культуре ткани (лимит Хейфлика), имеет другие механизмы клеточного старения (эффект изоляции). А вообще все жизненные проблемы связанные с провоспалениями тоже запускают механизм производства веществ из группы CD1, которые тоже могут вызвать или ускорить сенесцент.
Регуляция функций тимуса осуществляется и гормонами коры надпочечников (глюкокортикоидами). Таким образом, тимус имеет многовекторную регулировку и это объясняет почему некоторые односторонние меры влияния на него не дают радикальных решений.
Найден белок, который способен поддерживать молодость тимуса. Ученым удалось запустить неработающий в пожилом возрасте механизм замены старых клеток тимуса на новые. Для этого был использован белок, который вырабатывается клетками самого тимуса. Этот белок контролирует включение генов, управляющих функцией органа. Ученые увеличили концентрацию белка и так перепрограммировали клетки тимуса, что он омолодился.
Очевидно, это FOXN1 — особый белок, который помогает контролировать включение важных генов, управляющих функцией тимуса.
Также это же можно делать через стволовые клетки, однако их нужно было правильно активировать, чтобы они возместили возрастной ущерб. Для этого простимулировали белок FOXN1, который служит регулятором активности других генов. Активность самого FOXN1 сильно снижается с возрастом, так что понятно, почему исследователи выбрали именно его. Ген FOXN1 стимулировали у старых мышей, и в результате тимус мышей, бывший из-за возраста совсем крошечным, заметно увеличивался. Причём не просто увеличивался, но и начинал производить больше клеток. То есть его функция тоже восстанавливалась. Иными словами, удалось заставить орган регенерировать прямо в живом организме! Произошло это на фоне высокой степени гормональной зрелости, что, конечно, должно подавлять процесс регенерации. Поэтому, конечно, высокой степени и длительного процесса ювенилизации органа не достигнуть. Противодействует верхний этаж, отсутствие поддержки со стороны эпифиза. Следовательно, только двухстороннее воздействие окажет максимально высокий и устойчивый процесс омоложения.
Пересадка тимуса от молодого организма старому омолаживает. Во время одного из экспериментов двум собакам (старой и молодой) сделали операцию по пересадке вилочковой железы. Старому животному вживили молодую железу, а молодой собаке — старую. В результате первое животное очень быстро пошло на поправку, стало больше есть, активнее себя вести и вообще выглядеть на пару лет моложе. А второе быстро старело, дряхлело, пока не умерло от старости. Это связано с тимическими гормонами.
Введение мелатонина и синтетического пептида эпиталона, созданного на основе эпиталамина — вещества, выделенного из экстракта эпифиза, не только противодействует инволюции тимуса, но и даже омолаживает его. Результаты показали, что мелатонин отчетливо обращал вспять возрастную деградацию тимуса, о чем свидетельствовало заметное увеличение клеточной плотности и особенно количества тимоцитов и процентного содержания тимоцитов в фазах G2+S. Следовательно, инволюция не является необратимой, а также успешно корригируется интратимической имплантацией эпифиза. Восстановление морфометрических параметров сохранялось в течение 30 дней после прекращения приёма мелатонина, что свидетельствует о том, что восстановленный мелатонином гомеостаз может длиться довольно долго. Благодаря предварительной обработке клеточной культуры тимоцитов с 200 мМ мелатонина перед их обработкой гидроксильными радикалами (·OH), генерируемыми Fe2+, апоптотическая гибель клеток, вызванная ·OH, была почти полностью предотвращена. Как видим, апоптоз происходит в функциональных клетках — тимоцитах, что и является причиной дегенерации ткани. В данном случае апоптоз произошел как результат оксидативного стресса. Но в организме этот же процесс происходит благодаря неадекватной защитной реакции иммунных клеток на фоне различных изменений.
Экзогенный мелатонин, вводимый через желудочный зонд (5 мг/кг, перорально, через желудочный зонд) самцам крыс, модулирует окислительное повреждение тимуса и обращает вспять возрастную регрессию тимуса во время острой инфекции. Обращение возрастной регрессии тимуса проявлялось в увеличении массы тимуса, общего количества тимоцитов и в уменьшении возрастного накопления т. н. «двойных негативов» — незрелых Т-лимфоцитов. В целом ассоциированная с возрастом дисфункция иммунной системы характеризуется снижением уровня периферических Т-клеток, образующихся в тимусе, и потерей незрелых клеток линии B в костном мозге. Поскольку концентрация циркулирующего мелатонина уменьшается с возрастом, что коррелирует с возрастным ослаблением иммунной системы, в последние годы интерес был сфокусирован на иммуномодулирующем действии мелатонина. С иммунной системой связан сенесцент. Именно на эту сторону мелатонина автор возлагает большие надежды по противодействию дисфункциональной иммунной колее старения.
Эпиталон — геропротектор с противораковым эффектом. Повышает выработку мелатонина. Оказывает влияние на ночную выработку мелатонина, и его эффективность была в 500 раз выше, чем эпиталамина. Нормализует суточные ритмы выработки норэпинефрина и дофамина в гипоталамусе. То есть сдерживает старение гипоталамуса. От гипоталамуса зависят темпы сенилита во всём организме. Таким образом, действует одновременно и на сенесцент, и на сенилит.
Таким образом, введение экзогенного мелатонина или повышение секреции эндогенного нейромедиатора с помощью, например, эпиталона или препаратов со сходным действием могло бы найти применение в качестве эффективного подхода для стимулирования иммунитета, особенно у пациентов пожилого возраста [10].
Владоникс № 60 — пептид тимуса. Пептидный биорегулятор нормализует работу тимуса, или вилочковой железы, которая отвечает за иммунные клетки. Результаты применения Владоникса: восстановление клеточного обмена веществ, укрепление иммунитета, снижение аллергических реакций и заболеваемости, повышение защитных свойств организма.
Привыкания при применении Владоникса не происходит, потому что пептиды восстанавливают нормальную работу клеток и запускают процессы самовосстановления организма.
Владоникс рекомендован к применению людям, страдающим различными иммунодефицитами, как первичными, так и вторичными. Поскольку некорректная работа иммунной системы приводит к возникновению целого ряда заболеваний и к снижению сопротивляемости организма возбудителям болезней, её обязательно необходимо поддерживать в норме. Участвует в нормализации работы тимуса, вилочковой железы.
Очевидно, иммунометаболическое (трофическое и ювентализирующее*) действие тимуса возможно только при содействии высокого уровня гормонов эпифиза (мелатонин, эпиталон).
Снижение уровня половых гормонов уменьшает скорость деградации вилочковой железы. До полового созревания тимус функционирует усиленно (доминирует), и его гормоны подавляют активность половых желёз. Таким образом, тимус задерживает сроки полового созревания до наступления пубертатного периода [11]. Половые гормоны (андрогены и эстрогены) подавляют секрецию гормонов тимуса. Возрастное повышение уровня этих гормонов, а также вызванное беременностью увеличение уровня прогестинов приводит к резкой атрофии тимуса. Эти гормоны вызывают запрограммированную гибель тимоцитов, а эстроген (эстрадиол) дополнительно стимулирует атрофию тимуса. Росту тимуса и увеличению разнообразия иммунных клеток способствует угнетение или хирургическое разрушение гипоталамо-гипофизарно-гонадной оси. Однако в физиологических концентрациях половые гормоны (тестостерон, эстрадиол, прогестерон) и глюкокортикоиды, наоборот, усиливают выработку тимуса.
Эффект по элиминации всплеска гормонального фона можно получить с помощью гормона голода грелина. Этот гормон вырабатывается слизистой оболочкой желудка и вызывает чувство голода, действуя на центры гипоталамуса. Оказалось, что грелин участвует в Т-клеточном сигналинге, способен снижать связанное с возрастными изменениями воспаление, способствует восстановлению структуры тимуса и стимуляции его функций [12]. Т-клеточный сигналинг — процесс, который включает в себя получение, передачу и обработку сигналов Т-клетками для запуска иммунного ответа. Сенесцентные Т-клетки, например, могут способствовать развитию рака и ускорять сенесцент в Т-клетках и других. Голод модулирует иммунные клетки и систему.
Гормон роста обращает вспять атрофию тимуса и сохраняет его функции. В опытах на животных ученые уже обнаружили, что гормон роста способен остановить замещение тимуса жировой тканью. Выяснили, что комбинация веществ (гормон роста, метформин (препарат, который используют при сахарном диабете второго типа), дегидроэпиандростерон, цинк и витамин D) приводит к частичной регенерации тканей тимуса у человека и замедлению разрастания жировой ткани. Таким образом, иммунная система работает лучше, а биологический возраст человека уменьшается. Эксперимент длился два года. По окончании исследования ученые отметили увеличение числа Т-лимфоцитов в крови мужчин, а также регенерацию тканей, которые были замещены жировой. Средний биологический возраст после года приёма комбинации лекарств и веществ был примерно на 1,5 года меньше исходного. Проще говоря, организм не просто перестал стареть, он еще и помолодел.
Но при этом полного омоложения организма и возврата в стадию юности не происходило. Очевидно, в опыте не удалось привести к комплексному доминированию гормонов юности над гормонами зрелости.
В то же время запускать в организме слишком высокие уровни гормона роста тоже рискованно, так как это может привести к акромегалии (диспропорциональный рост частей тела) или юношеской акселерации (гигантизм).
Глюкокортикоиды вызывают острую деградацию вилочковой железы. Разрушающе действуют как препараты этого класса, например, дексаметазон, так и глюкокортикоиды, вырабатываемые самим организмом. Например, при стрессе или при нарушении механизмов регуляции функции надпочечников вырабатывается чрезмерное количество гормона кортизола — естественного глюкокортикоида.
Вирус гриппа А вызывает атрофию тимуса, повышенную гибель незрелых иммунных клеток и снижение их разнообразия. Столь же разрушительно на вилочковую железу влияют и бактериальные инфекции, например, стрептококковая.
Старение организма характеризуется снижением функций иммунной системы. Главная причина этого снижения — деградация тимуса. В результате нарушается процесс созревания иммунных клеток и уменьшается их разнообразие. В организме пожилых людей накапливаются стареющие иммунные клетки памяти, которые приводят к хроническому воспалению. Тимус подвергается постоянному возрастному старению вне зависимости от своей способности к омоложению.
Стареющие иммунные клетки памяти приводят к хроническому воспалению, а через него к неизбежному синдрому хронической усталости (СХУ). Это начало всех начал, в том числе сенесцента и сенилита. Это тлеющий огонь, который постепенно разгорится в пожар анизомалий. Через иммунную систему организм включает старение, а затем подводит к мортусу.
Показаны связи между возрастной деградацией вилочковой железы, иммунным старением и хроническим воспалением. Доказана решающая роль этих процессов в прогрессировании возрастных неврологических, сердечно-сосудистых и онкологических заболеваний.
Старение иммунной системы обуславливает старение организма
Среди всех 16 систем организма иммунная система стареет первой. Через врождённую иммунную систему запускается одна из основных характеристик старения, а именно за усиление вялотекущего воспаления, известного как «воспаление старения».
Как тимус замедляет старение? Кроме подготовки «спецназа» Т-лимфоцитов он вырабатывает тимические гормоны, которые способствуют регенерации, восстановлению и активируют работу иммунной железы. Тимус выделяет в кровь биологически активные факторы: фактор роста, снижающий уровень кальция в крови в крови, инсулиноподобный фактор роста, который снижает концентрацию кальция в крови. Одним словом тимус работает на омоложение организма.
Старение и воспаление (Inflammaging) [13]
Одной из основных характеристик старения является хроническая активация иммунной системы, которая приводит к вялотекущему воспалению, в основном вызванному макрофагами. Активация иммунной системы запускает механизмы сенесцента у подшефных клеток. Старение происходит не из-за тотального сенесцента, а из-за настройки иммунной системы на сенесцент. Иммунная система подталкивает, направляет подшефные им клетки на сенесцент. Стареющие клетки выделяют множество факторов, которые называют «секреторным фенотипом, ассоциированным со старением» (SASP). Медиаторами этого системного воспаления являются провоспалительные цитокины, такие как интерлейкин-6 и фактор некроза опухоли альфа…, уровень которых повышается с возрастом [14]. Эти медиаторы являются не просто причиной хронического воспаления и сенилита, но и целенаправленными факторами, через которые реализуются многочисленные анизомалии (запредельно высокая и поголовная «заболеваемость» неизлечимой хроникой), и мощными рычагами, механизмами, ведущими к мортусу (смертности) пожилых людей. Мортус и анизомалии — это не случайности сенилита, а направленный акт реализации феноптоза, самоуничтожения. Считается, что основная цель выработки SASP — активировать клетки врождённого иммунитета, такие как макрофаги, чтобы они фагоцитировали стареющие клетки, вырабатывающие SASP, и тем самым предотвращали развитие опухоли [15]. SASP включает в себя факторы роста, провоспалительные цитокины, хемокины и протеазы, которые могут способствовать развитию воспаления при старении. НО! Автор считает, что первыми стареют иммунные клетки, что связано триггерно с изменениями в тимусе, эпифизе и гормональном фоне. Происходит это через стареющие иммунные клетки с фенотипом памяти. Очевидно, с инволюцией тимуса закрепляется феномен фенотипа памяти. Причём фенотип памяти связан не только с внешними факторами, но и эндогенно. В тимусе происходит ювентализация* этих клеток. Без тимуса невозможно держать баланс доминирования ювентальных над сенесцентными клетками.
Гормоны тимуса. К основным гормонам тимуса относятся тимозин, тимопоэтин и тимулин.
Тимозин непосредственно воздействует на клетки, обладающие иммунной реактивностью. Механизм действия тимозина основан на стимуляции лимфопоэза.
Тимопоэтин в первую очередь контролирует дифференцировку Т-лимфоцитов. Он также усиливает экспрессию проопиомеланокортина, секрецию продуктов его процессинга — АКТГ, p-эндорфина и p-липотропина, а также СТГ и кортизола.
Как видим, иммунная система через Тимопоэтин участвует в экспрессии гормонов стресса, роста и…
Гормоны, находящиеся под контролем гормонов тимуса и являющиеся соучастниками в проявлении поседения волос — как маркера сенилита
Проопиомеланокортин (POMC) — полипептид-предшественник, который расщепляется с образованием множества пептидных гормонов. Некоторые из них и их функции:
- α-меланоцит-стимулирующий гормон (α-MSH). Играет важную роль в регуляции аппетита (стимуляция нейронов POMC приводит к ощущению сытости) и сексуального поведения. Также регулирует движение меланина, вырабатываемого меланоцитами в коже;
- адренокортикотропный гормон (АКТГ). Регулирует секрецию глюкокортикоидов из клеток пучковой зоны коры надпочечников. Также может регулировать секрецию гонадокортикоидов клетками сетчатой зоны;
- β-эндорфин и энкефалин. Являются эндогенными опиоидными пептидами, широко действующими в головном мозге;
- проопиомеланокортин участвует в регуляции многих процессов, включая энергетический гомеостаз и метаболизм, стрессоустойчивость, пигментацию и воспаление. Пигментация волос является лучшим маркером сенилита в целом и сенесцента клеток меланоцитов.
Омоложение эпифиза
Концепция такая: если нам удастся перезапустить работу эпифиза во взрослом состоянии, то это позволит повернуть цепочку развития процессов в нём в обратном направлении, а значит, омолодить гипоталамус и гипофиз. Но это всего лишь концепт. Так как можно предположить, что существующий высокий уровень половых гормонов все равно будет подавлять эпифиз. Но тем не менее экзогенный мелатонин может постепенно снизить гиперфункцию гипоталамуса, а это откроет сигналинги по возрождению эпифиза. Высокий уровень половых гормонов подавляет, снижает уровень мелатонина. Они антагонисты. С уровнем половых гормонов сопряжены и другие гормональные железы, такие как щитовидная железа и др. Так что процесс перестройки будет происходить синхронно и в других железах.
Известно, что в эпифизе у человека уже к 6–7 годам образуются камнеподобные отложения, когда клетки его кальцинируются. Это указывает на метавоспаление и сенесцент в нём уже в раннем детстве! Следовательно, в эпифизе происходит не только угасание функции, но и дегенерация ткани и кальциноз.
Очевидно лучше всего с ним могут справиться антиинфламанты (лютеолин, куркумин…?), аутофагия и автономия. Вытащить избыточный кальций поможет приём высоких доз Mg (см. рис. 5).
 МАГНИЙ ЦИТРАТ ЭКСПРЕСС ФОРТЕ ВИТАУКТ
МАГНИЙ ЦИТРАТ ЭКСПРЕСС ФОРТЕ ВИТАУКТ
Рис. 5. Почему с возрастом у людей не хватает Mg? Анализы часто могут показывать норму Mg в плазме, но при этом его может существенно не хватать в костной и других тканях, функциональность которых сильно связана с Mg. Сенесцентные клетки попросту резистентны и не используют его в достаточных количествах. Это связано с их пониженной энергетикой и гликолизностью. Снижает уровень скрытого стресса и улучшает сон. Помогает восстановить энергетику сенесцентных клеток, так как участвует в выработке АТФ митохондриями.
Любой эффект магния или кальция зависит от соотношения кальций/магний. Если в крови достаточно магния, то он стимулирует образование гормона кальцитонина, который и обеспечивает вход кальция в кости, без этого кальций остается в плазме и повреждает другие ткани. Магниевый дефицит становится нормой поголовно у взрослых и стареющих людей, особенно при климаксе и многочисленных хронических возрастных заболеваниях, стрессе. Выявлена защитная роль магния при кальцификации сосудов.
Кальциноз также всегда проявляется в местах с высоким уровнем провоспаления. Гасить провоспаление поможет лютеолин (см. рис. 6).
 ЛЮТЕОЛИН
ЛЮТЕОЛИН
Затем нужно помочь процессам регенерации ткани, и апоптоз или сенолитики должны сыграть свою роль. Но нужно запустить и репарацию. Для омоложения эпифиза и поддержания его активной работы используют пептидные биорегуляторы. Это белковые соединения, которые несут в себе информацию о правильной работе клетки и запускают процесс регенерации.
«Эндолутен» — один из таких препаратов. В его состав входят пептиды, выделенные из эпифиза молодых животных. Препарат восстанавливает работу шишковидного тела на клеточном уровне, замедляет процессы старения и увеличивает продолжительность жизни.
«Эпиталон» — аналогичный препарат.
Другой препарат на основе пептидов для тканей эпифиза — «эпифамин». Он содержит пептиды, регулирующие метаболизм клеток эпифиза.
Только на этом фоне можно применять высокие дозы мелатонина, чтобы снять доминирование гипоталамуса над эпифизом. Очевидно, дозы должны быть не менее 25 мг/сутки.
Вегетативная нервная система и роль её симпатического и парасимпатического отделов в поддержании ювенильности или сенилита эпифиза
Эпифиз с возрастом подавляется через симпатическое крыло вегетативной системы. Омоложение эпифиза возможно с помощью усиления парасимпатики и подавления симпатического отдела. Симпатический отдел является стороной активации, связанной со стрессом, и подавляет эпифиз как в плане его гормональной активности, так и иммунной, то есть ускоряет его старение.
Самый сильный активатор симпатики — это свет, поэтому рекомендуется увеличить период темнового пребывания организма, то есть поменять актиноритмы* [16].
Примером, подтверждающим возможность омоложения или сохранения молодости через эпифиз, являются случаи, когда люди впадают в длительную кому, что способствует полной остановке стимуляции эпифиза через симпатическую нервную систему, при этом даже спустя десятилетия у них остановилось старение. Этот феномен зафиксирован и так и не осознан наукой.
Централизация процессов УКАМ в ОАС
Важен ответ: кто запускает во всей этой массе различных резидентов сенесцент, причём в разное время? Происходит цепная реакция: от одних тканей идёт процесс передачи инициирования в другие. Постепенно процесс из локальных участков переходит на общеорганизменный, тотальный, когда подключается и иммунная система крови, и тоже усиливает цитокиновый выброс провоспаления. В итоге происходит переход с уровня УКАМ на ОАС, что проявляется в старческой немощности, синдроме СХУ, саркопении…
Через механизмы УКАМ и ОАС сенесцент запускает сенилит
Довольно известно, что ОАС спускается вниз на клеточный уровень, но плохо понят переход, восход с первичного клеточного уровня на общеорганизменный.
Сенилит усиливает сенесцент через эти же механизмы ОАС в УКАМ
Всё осуществляется через неспецифические стороны ответов иммунной системы и сопряженных с ней других механизмов регулировок.
Многоступенчатое, многоэтапное взаимодействие: 1) сенесцент ⇔ сенилит; 2) сенесцент ⇔ сенилит; 3) сенесцент ⇔ сенилит… = геронтос. Всё начинается с сенесцента в тимусе, затем в эпифизе…, а заканчивается тотальным сенилитом.
НО! А если остановить сенесцент эпифиза? Организм будет на длительной ювенально-вегетирующей фазе роста. Возможно несколько вариантов проявлений, в том числе и проявление неотении* [17]. В одном из таких вариантов процесс может реализоваться через механизм гипофизарного нанизма. В этом случае гипофиз резистентен к сигналам гипоталамуса по соматотропному и гонадотропному релизинг-фактору. Как результат недовырабатываются гормоны половые и роста. Но, очевидно, это ведёт к тому, что растормаживается эпифиз и выделяет повышенное количество мелатонина. Гормональное торможение эпифиза не происходит, исключён его сенесцент. Повышен мелатонин — дорога к неотении. К тому же ряд научных работ прямо показывают, что мелатонин выступает как средство против старения при возрастных заболеваниях (анизомалиях) [18].
Является ли сенесцент проявлением одной из модификаций (сенесцентным аналогом фенотипов), в первую очередь иммунных клеток?
Наука пока говорит, что это разные процессы. Тем не менее автор утверждает, что сенесцент связан с многими механизмами фенотипических модификаций. Фенотипы, модификаты, сенесцент тоже реализуются через эпигенез и тоже сцеплены с тем же блоком генов. В отличие от обычных иммунных фенотипов (М1, М2…), при сенесценте эта фенотипия переходит в устойчивую модификацию (невозвратную, то есть изменения происходят в большей степени не со стороны функциональных возможностей, а структурно). Это уже фаза не просто активации, а гиперактивации иммунных клеток. В этом режиме они выходят за рамки гомеостазов, становятся резистентными, не подчиняемыми (сенесцентными). Фенотипические изменения переходят в модификационные.
Чем отличается фенотип от модификата?
Создаются клетки с новым гомеостазом с новыми правилами, противоположными прежним. Этот гомеостаз с большей автономией и сам себя поддерживает, меньше управляем, выше резистентность. Такие модификаты имеют большую устойчивость и живучесть. Модификаты прорвали границу гомеостаза и перекрыли возврат к прежним фенотипам. Базируются они на принципах гликолиза. На первом месте у них задача — выживать самим, а не обеспечивать стем-клетки. Меняясь сами, они меняют статус и стем-клеток.
Понятие модификат* ввёл Г. А. Гарбузов. Для их различия предложено им дать свои обозначения: ММ1… Очевидно, что онкологические клетки тоже связаны с модификатом сенесцентных иммунных, но с высокой репликационной способностью, и их следует обозначить как ММ2. Стволовые раковые онкоклетки регулируются иммунными.
Многочисленные данные позволили автору утверждать, что: сенесцент — это результат активности модифицированных макрофагов. Причём если для появления фенотипов макрофагов важны внешние факторы, то для модификатов важны больше внутренние факторы клеток (стресс, исходящий изнутри клеток на фоне гормоно-, иммуно-, нейроперестроек). Таким образом, сенесцент не является следствием лимита Хейфлика, а сам лимит Хейфлика является результатом стресса для клеток при содержании их в отрыве от всего организма.
Внешние и внутренние факторы для клеток для появления фенотипов и модификатов
Ряд авторов считают, что чтобы омолодить клетку, нужно воздействовать не на сами клетки, а на окружающую их среду (очевидно, подразумевается секретом, в т. ч. и SASP). Но при этом авторы понимают, что старение клетки связано со средой, в которой они живут. Но сама среда крови созревшего организма является условием для перестроек клеток изнутри, им попросту становится «некомфортно», и они вынуждены перестраиваться. Образование фенотипов и модификатов всегда проходит через изменение среды клеток. Только в одних случаях эту среду меняют внешние факторы (с появлением М1, М2…), а в других — перестройки изнутри клеток и изменение их секретома (с появлением ММ1, ММ2…). Это означает, что через эту среду для клеток можно вести коррекции в отношении М1, М2…, ММ1, ММ2… и вплоть до запуска механизма ювентального реверса* (для клеток) и ювенилизации всего организма.
Среда клеток меняет их матричные структуры. Например, когда старые клетки сердца с жесткой матрицей помещали в гидрогель с биохимической средой, близкой к молодым клеткам, они начали вести себя как молодые: изменилась активность тысяч генов, связанных со старением и клеточными функциями. Биохимическая среда играет ключевую роль в старении. Этот механизм очень схож с процессом парабиогенеза*, когда молодые клетки при их доминировании способны омолаживать старые и, наоборот, когда старые переводят молодые в старые.
Кстати, мелатонин — гормон, который регулирует гомеостаз в микроокружении.
Возможности мелатонина в противодействии сенилиту и сенесценту
Многие работы указывают, что мелатонин перспективен для замедления процессов старения и связанных с ними заболеваний, включая сердечно-сосудистые и нейродегенеративные расстройства.
Мелатонин работает не только на общеорганизменном уровне (сенилит, через ремодификацию в эпифизе), но и на клеточном (сенесцент). Длительное лечение пожилых крыс мелатонином не только улучшает функцию митохондрий, но и:
- снимает дисфункцию митохондрий (то есть даже в уже сенесцентных клетках происходит возврат в исходное состояние);
- подавляет активирование (фенотипическую поляризацию) макрофагов М1 [20], а значит, и образование устойчивых модификатов (сенесцентоподобных), а через провоспалительные модификаты происходит устойчивое угнетение стем-клеток*, что означает и функциональную слабость этих тканей, или, другими словами, утрату Жизненной Силы;
- снижает провоспаление в организме;
- осуществляет модуляцию пути сиртуина 1 (тем самым содействует ремодификации и ювентализации макрофагов);
- модуляцию аутофагии, которая снижается с возрастом;
- экзогенный мелатонин эффективно снижает повреждения ДНК, вызванные старением, оказывая антигенотоксическое и антимутагенное действие;
- может быть рекомендован как при всей хронике с провоспалениями, так и всех анизомалиях*.
Обращает на себя внимание, что мелатонин способен останавливать модификацию макрофагов М1 [21], а ведь это путь не только к заболеваниям, но и к сенесценту через макрофаги! Путь сенесцента и хронических заболеваний реализуется на одних и тех же иммунных механизмах. Через сенесцент макрофагов в эпифизе осуществляется переход от этапа юности и детства к пубертату*, а затем к адальтусу* и матуре*, с выходом на геронтос* и мортус*.
Автор предполагает, что мелатонин помогает перевести макрофаги из статуса модификатов (сенесцентоподобных) в статус фенотипов, которые более работоспособны. Имеется в виду, что сенесцентные макрофаги подавляют стем-клетки, тогда как фенотипические повышают их работоспособность.
Это указывает на то, что мелатонин должен входить в Комплексные Программы по анти-эйдж. Таким образом, мелатонин является важнейшим компонентом в Программах по преодолению модификатов и сенесцента. Цель поставленных задач — запустить механизмы реювенилизации (Витаукт) через механизмы клеточного ювентального реверса* (Жизненная Сила).
Кстати, мелатонин не может синтезироваться из серотонина без витамина D. Но возрастной эпифиз сенесцентен и резистентен к серотонину и витамину D. Восстанавливать его (реювенилизировать и реювентализировать) поможет экзогенный мелатонин в высоких дозах (20 мг/сутки) в течение 18 месяцев. Но важно запускать, стимулировать работу самого эпифиза с помощью высокого фона триптофана (предшественника серотонина) и витамина D (см. рис. 7).
 ВИТАМИН D3 ЭКСПРЕСС ФОРТЕ
ВИТАМИН D3 ЭКСПРЕСС ФОРТЕ
Рис. 7. Всего 2000 МЕ витамина D в день достаточно, чтобы снизить скорость укорочения теломер почти в три раза и тем самым замедлить старение. Витамин D3: фундамент антивозрастной метаболической терапии. Только в условиях высокого фона витамина D3 мелатонин может вырабатываться из серотонина, а серотонин — из триптофана. Мелатонин способствует реювентализации за счёт снижения резистентности сенесцентных клеток. Способен резко замедлить скорость старения нашего организма. Повышает выработку белка молодости-ювентальности Клото. Обнаружена связь между приёмом витамина D и скоростью укорачивания теломер — защитных «колпачков» на концах хромосом. Именно их длина считается одним из ключевых маркеров биологического возраста.
Мелатонин выведет макрофаги из состояния модификатов в фенотипы. В первую очередь надо снять сенесцентность и резистентность.
В этом же направлении по восстановлению стем-клеток или = клеток-функционала окажет помощь приём магниевого препарата в цитратной форме.
Повышение эффекта мелатонина с помощью лютеолина
Следует ожидать, что такие комбинации позволят снизить дозировки лютеолина, повысить чувствительность клеток к нему.
Гомойотопические* механизмы сенилита
Так при отключении механизмов сенесцента эпифиза (активаторов его ингибирования) организм может пойти по пути пойкилотопии* [19] — принцип существования древних животных, когда не было ограничения размеров животных, а многие виды из них достигали гигантских размеров, неоптимальных для существования и видовой целесообразности. Да, многие такие животные с такими программами даже сейчас существуют и могут достигать огромных размеров (акулы, галапогосские черепахи), доживать до 400 лет. Умирают они не от старости, или старость у них по другим причинам.
Также в усилении сенесцента участвует гомойотопия* — механизм торможения роста. Это нужно для сохранения размера организма. Гомойотопия связана как с центральными механизмами гормональной регулировки процессов роста, так и с усилением модификации и сенесцента иммунных клеток, которые вызывают торможение активности стволовых клеток в точках роста и даже их вырождение. Эти точки роста становятся резистентными и попадают в режим гипоксии и провоспаления.
Омоложение (ювенилизация ткани или ювентализация клеток) на одном уровне организма (верхнем или клеточном) в одностороннем порядке невозможно
Это единая система, где каждая сторона будет противодействовать другой. Омоложение возможно только при одновременном изменении процессов геронтоса на двух уровнях (сенесцент и сенилит), а именно омоложение главного драйвера — эпифиза, а затем омоложение на нижнем уровне клеток. Омоложение клеточного уровня должно привести к возобновлению работы эпифиза. Но напомню, что эпифиз стареет-сенесцентирует первым. Снятие ограничительных тормозов в нём приведёт к обратной трансформации работы гипоталамуса, значит, устранению сенилита. Это опять повысит уровень вегетативных гормонов и понизит уровень репродуктивных. Чем это может закончится в сформировавшемся организме? Не запустит ли это продолжение фазы роста? Возможно, здесь нужно будет умело манипулировать одновременно и процессами катаболизма, аутофагии и апоптоза с помощью особых методик голодания, ускорения процессов метаболизма с целью более быстрого устранения или обратной модификации сенесцентных клеток.
Универсальность процессов сенесцента в разных тканях
Механизмы сенесцента в разных тканях одни и те же. Это означает, что методики антисенесцента, которые проявили себя положительно в одних тканях, окажут такое же действие и в других, например, в эпифизе.
Пример антисенесцентного действия лютеолина в направлении восстановления цвета волос при их поседении. Появились данные, показывающие, что поседение волос возможно устранить с помощью лютеолина [22]. Это означает, что если добиться можно антимеланопении (в луковицах волос поседение), то эти же методы и препараты будут помогать и от пинеалопении и от...
Дозировки и сроки применения лютеолина для достижения эффекта антипоседения, а также десенесцентизации (реювенилизации) эпифиза
В опытах на мышах для достижения эффекта антипоседения его нужно было принимать в гипердозах (3 г/день). По срокам эффект проявлялся через 6 недель. Если длительность жизни человека 80 лет, а у мыши 2,5 года, то эффект у человека должен проявиться через 32 недели, или 8 месяцев. Но, очевидно, для реювенилизации эпифиза (трансформации) ткани явно этих сроков будет недостаточно. Для того чтобы произвести реювенилизацию, предварительно нужно достигнуть резорбции в нём кальцинации и дегенерации (вырождения), то есть для достижения по сути регенерации явно следует ожидать более длительных сроков, не менее 1–1,5 года.
Важно при этом понимать, что одному лютеолину с этой многоплановой задачей не справиться. Нужны будут комбинации, включая мелатонин и др.
Сможет ли лютеолин снять сенесцент в эпифизе?
Да. По гипотезе автора, механизмы сенесцента реализуются через иммунную систему и метавоспаление, которые во всех тканях одни и те же. Лютеолин должен подавлять сенесцент и в эпифизе — главном органе, запускающем сенилит.
Почему для антисенесцентного эффекта нужны гипердозы лютеолина?
Лютеолин работает как антипровоспалитель и антиоксидант, а в больших дозах он прооксидант, а значит, активирует оксидативный стресс. Но почему его нужно принимать в прооксидантных дозах? Возможно, только так он устраняет сенесцентные клетки, работает как сенолитик*. Значит, сенесцентные клетки первыми не выдерживают гипероксидативный стресс и апоптируют.
О важности, кроме сенолитического воздействия, ремодифицирующего сигнала
Казалось бы, после сенолитиков на месте сенесцентных клеток должны появляться ювентальные. Но так ли это? В культурах ткани сенесцентные клетки при простом оксидативном стрессе просто вымирают. Мешает парабиогенетический* эффект самосохранения от одних старых клеток для других. Очевидно, для ювентализации нужен сигнал, который связан с ремодификацией. Не является ли лютеолин и сигналом для одновременной ювентализации через ремодификацию?
Некоторые исследования показывают, что лютеолин может действовать против сенесцентных клеток.
Г. А. Гарбузов расценивает лютеолин как генетический важный универсальный «переключатель» провоспаления как на местном уровне (врождённый иммунитет из макрофагов in situ), так и на системном, общеорганизменном (подвижные иммунные клетки лимфоциты). Лютеолин блокирует-регулирует-балансирует сотни генов, связанных с провоспалением. Очевидно, это и является ключом к ремодификации сенесцентных иммунных клеток. Таким образом лютеолин действует двойственно: с одной стороны, он сенолитик, а с другой — ремодификатор. Возможно, ремодификация (достижение омоложенного статуса) — более важный процесс, чем сенолитизм.
В частности, есть информация, что лютеолин подавляет вызванное H2O2 старение клеток (сенесцент) посредством модуляции SIRT1 и p53. Также есть данные, что лютеолин способен подавлять процесс возникновения седины (индикатор сенесцента и сенилита). Также есть данные, что мелатонин тоже работает в направлении ремодификации при сенесценте. Например, мелатонин способен контролировать пигментацию и рост волос, а его дефицит может приводить к появлению ранней седины.
Эффект связан с влиянием лютеолина на эндотелины — белки, которые играют важнейшую роль в межклеточной коммуникации.
Иммунная система является осью, интегрирующим звеном для всех уровней регулировок
Её действие в одних условиях реализуется через трофическую активность и контроль гомеостаза тканей, а также защитную функцию, а в других — через провоспалительные механизмы и вплоть до уничтожения своих подшефных клеток. Провоспалительная сторона может играть роль как сигналов SOS для системной централизации защитных ответов (специфических и неспецифических), так и для самореализации феноптоза*, самоуничтожения. Эволюцией предусмотрена для каждого вида своя продолжительность жизни (онтодианная линия), а также то, что ослабленные хроникой организмы должны самоэлиминироваться.
Сенесцент стем-клеток осуществляется через сенесцент иммунных клеток-регуляторов пролифераций (КРП*)
Осуществляется это целенаправленное самоэлиминирование иммунными клетками через подавление, ограничение, лишение Жизненной Силы в стем-клетках. Стем-клетки стареют (сенесцентируют) не сами, а их заводят на этот путь иммунные клетки-регуляторы (КРП*) (предварительно модифицированные). Сенесцент наводится с двух этажей:
- за счёт КРП (локально),
- за счёт интервенциональных процессов (глобально), в частности белка сенесцента ReHMGB и SASP.
Любой рост соматических клеток сопровождается пролиферацией КРП и наоборот: при возрастном снижении активности КРП снижается и уровень фонового потенциала роста тканей, но это регуляторный и принципиально обратимый процесс.
КРП решает задачи интеграции многоклеточного сообщества в единый организм.
- Ведущим механизмом старения соматических тканей является снижение их клеточного самообновления.
- Снижение потенциала клеточного роста соматических тканей при старении определяется изменениями в системе лимфоидной регуляции пролиферации соматических клеток.
- Сущностью изменений КРП* в старости является увеличение доли КРП ингибиторов и абсолютное снижение общего числа КРП.
- Нарушение соотношения КРП стимулирующего и ингибирующего типов ведет к снижению скорости продвижения соматических клеток из фазы G1 в S, формируя G1/S блок в тканях старых животных.
- Прогрессирующее снижение пролиферативной активности клеток соматических тканей ведет к увеличению доли "старых" клеток, при этом "старческие" изменения являются результатом проявления нормальных свойств таких, углубившихся в состояние дифференцировки, клеток с длительным периодом жизни.
- Так как в тканях всегда идут процессы замещения молодыми клетками, наряду с процессами старения формируются процессы приспособления, гипертрофии и пр.
- Изменения системы КРП являются результатом продолжения действия регуляторов ограничения роста организма после того, как ост закончен, при участии гипоталамо-гипофизарной системы и тимуса.
- Возрастной иммунодефицит связан с выраженным снижением потенциала роста тканей и снижением реакции КРП в ходе рост-индуцируемых процессов. Ограничение потенциала роста в ряде тканей связано с кейлонными механизмами ограничения роста изнутри клеточных популяций.
Лимфоидная теория старения
Можно полагать, что при старении резко снижается функция Т-лимфоцитов-КРП системы как результат изменений в регуляторных системах организма.
2. Важнейшим уровнем такой регуляции является система межклеточной регуляции клеточного роста разнотипных соматических тканей.
3. Рассмотрение экспериментальных данных иммунологии и клеточной биологии показывает, что такая система может быть представлена специализированными Т-клетками - стимулирующих и ингибирующих популяций, реагирующих в "сингенной смешанной культуре лимфоцитов" на собственные растущие клетки организма.
4. Снижение функции таких Т-регулирующих клеток с возрастом может являться центральным механизмом для старения самообновляющихся соматических тканей организма и определять снижение с возрастом ростового потенциала тканей старого организма.
Значение иммунной системы для повышения уровня зрелости и функциональности высших регулировочных центров
Через иммунную систему трансформируется («созревает») работа высших центров регулировок (элевация гипоталамуса, эпифиза), а затем инициируется резистентность (нечувствительность) в тканях in situ, в том числе и в тканях-железах мишенях. Это является прологом для созревания и перезревания (переходом из ювенильной в репродуктивную фазу пубертата, а затем усиления адальтуса* и матуры*) с последующей инволюцией центров регуляции. Причём элевация, гиперэлевация и инволюция происходят не параллельно во всех центрах регуляции, а путём усиления одних центров и отключения других. Например, угасает работа эпифиза, но резко усиливается работа ряда центров гипоталамуса.
Подавление роли ювентальных клеток, но активирование роли сенесцентных клеток — причина исчерпания резервов и угасания клеточной Жизненной Силы, а затем и Витаукта
Ювентальные* клетки и их толерантность (устойчивость, сопротивляемость) подавляются, но на этом фоне в организме постоянно нарастает резистентность в связи с усилением роли стареющих клеток. Стареют (модифицируются) в первую очередь иммунные клетки. Вслед за этим слабеет Жизненная Сила стем-клеток. Модификация иммунных клеток и трансформация стем-клеток (то есть ослабление Жизненной Силы) в ведущих тканях ведёт к подавлению Витаукта на уровне всего организма (сенилит). Подавление Витаукта реализуется через систему как анизомалий*, так и анизопений*.
Взаимодействие ювентальных и сенесцентных клеток
Таким образом, сенесцентные иммунные клетки способствуют старению, в то время как «молодые» иммунные клетки ему противодействуют. Если сенесцентные клетки работают через SASP, то ювентальные должны работать через UASP* — свой ювенильный спектр секретома (понятие предложил Гарбузов Г. А.). Сюда же входят и SIRT1 (сиртуины — гены долголетия). В норме в юности между сенесцентными и ювентальными клетками происходит баланс их секретомов и модификатов в пользу ювентальных, они доминируют и определяют ситуацию, состояние ткани. Смена UASP на SASP является дистрессом на клеточном уровне. Метавоспаление является основой для резистентности клеток и запуска эпигенеза на сенесцент. Ювентальная не модифицированная иммунная система элиминирует почти все сенесцентные клетки, но с возрастом возможности ювентальной иммунной системы подавляются путём их модификаций. Появились данные, что иммунная система с возрастом не только хуже справляется со своими функциями, но и сама становится активной причиной старения всего организма [23]. Стареющие клетки иммунной системы способны активировать сенесценцию в здоровых тканях.
Сенесцент и сенилит — неминуемый механизм запуска мортуса
Мало того, эти же механизмы старения через цитокины и анизомалии запускают неизбежный механизм мортуса.
Центральные механизмы подавления ювентального типа иммунитета
С возрастом изменяются:
- гормональный профиль,
- медиаторный фон,
- иммунный фон,
- усиливается прессинг со стороны механизмов гомойотопии*.
Все они воспринимаются как стресс и влияют на баланс ювентальных клеток, но усиливают сенесцентные. Так верхние этажи вмешиваются в статус нижних этажей, снижая в них резистентность, а значит, повышая сенесцентность.
Внешние изменения переходят во внутренние, что приводит к смене UASP* (ювентальный секретом) на SASP (сенесцентный секретом).
По сути, смена UASP на SASP или обратное SASP на UASP является механизмом аутопарабиогенеза* (самосостаривание или самоомолаживание). Это означает, что смена секретома на обратный приведёт к обратному парабиогенезу.
Но внутренние изменения в клетках зависят от изменений внешнего фона. Сможем ли мы изменить внешние изменения для клеток? С другой стороны, внешние изменения зависят тоже от внутренних перестроек. Очевидно, важно удерживать изменения внешнего профиля и внутреннего профиля до наступления критических точек. Эти пороги находятся в ранней юности (допубертат).
Большую роль в парабиогенной поддержке ювентальности может иметь пища с высоким уровнем UASP.
Основные направления подавления геронтоса (старения)
Изложенное указывает чётко на то, что сдерживание геронтоса должно вестись одновременно с двух направлений:
- верхнего (центральной регулировки),
- нижнего (иммуно-клеточного).
Такой комплексный подход на основе интегрированного взаимодействия и взаимовлияния разных этажей регулировок (гомеостазы определяют гормезис, а гормезис определяет гомеостазы) в корне отличает предлагаемую автором гипотезу от всех подобных, но с односторонним подходом. Это же означает, что Жизненная Сила определяет Витаукт, а Витаукт определяет Жизненную Силу. Это же означает, что сенесцент определяет сенилит, а сенилит определяет сенесцент. Клетки стареют не сами по себе (в связи с укорочением теломер или лимитом Хейфлика), а их наводят на этот путь путём изменений во внешнем фоне (по мере роста или созревания) для них и реакцией иммунитета на эти изменения.
Особо большое внимание верхнему этажу (гормональной корректировке) как причине старения уделял Дильман В. М. [24]. Позже появился ряд работ, проясняющих значимость нижних клеточных этажей как причин старения [23, 1]. Тем не менее в них так и не были осознаны системность процесса и интеграция верхних и нижних этажей становления регулировок старения.
Механизмы онтогенеза, эпигенеза, нейро-гормоно-иммунного созревания, сенилита и гомойотопии*, а также патологий создают условия для гиперактивации иммунных клеток (врождённого и приобретённого иммунитета: макрофаги, нейтрофилы и др.). Это ведёт неизбежно к усилению производства провоспалительных цитокинов (например, IL-6 и множества других субстанций), а заодно представляет новый секретом и функциональный протеом.
Выход за пределы оптимального режима работы гомеостаза — путь к сенесценту (сенесцентной модификации)
В норме сенесцентные модификации должны постоянно элиминироваться. Это и происходит, но только в юности. В более поздние этапы иммунные клетки становятся резистентными. Их реювенилизации мешают факторы возрастных изменений. Сенесцентно-резистентные клетки становятся доминирующими над ювентальными.
Сенилит и общеорганизменные перестройки регулируют сенесцент
Возможности такой элиминации с возрастом гаснут из-за подключения возрастных факторов на общеорганизменном уровне. Одним из таких факторов является период неполовозрелости и роста организма. Например, допубертатный период у животного голый землекоп в разы больше, чем у мышей, что сказывается на многократном увеличении продолжительности жизни при сохранении одинаковых размеров. При этом и сенесцент клеток у голого землекопа наступает значительно позже. Определяет их сенесцент не лимит Хейфлика, а длительность этапа ювенильности, то есть длительность сохранения особого гормонального фона. Гормональные факторы сенилита здесь надолго отодвинуты, а эпифиз долго работает как у молодого. Сенесцент у мышей начинается очень рано (через 8 месяцев), тогда как сенесцент у землекопа запускается через многие годы. Всё зависит от коммитированной (изначальное предписание) генной настройки чувствительности сенсоров иммунных клеток-резидентов в эпифизе на изменение в параметрах некоторых гормонов. Если проще говорить, то чем быстрее стареет эпифиз, тем быстрее стареет и организм. Через иммунные клетки идёт подавление функции эпифиза по поддержанию ювенильности, дополовозрелости. У одних животных эпифиз изначально настроен на длительное функционирование и длительную фазу ювенильности, а у других — на короткое функционирование и быстрое созревание.
Возможно, если мы научимся регулировать степень сенесцента в эпифизе, поддерживать его функционал, мы сможем продлить в разы этап человеческой юности (неотении) и продолжительность жизни. Напомню, что продолжительность жизни землекопа в 10 раз выше, чем у мышей. Предполагаю, что и человек тоже имеет возможность раздвинуть границы своей жизни в 10 раз.
Отодвижение зрелости и старения (сенилита) регулирует и отодвигает сенесцент
На это указывает вышеприведенный пример с животным голый землекоп, а также то, что сенесцент — это не независимый процесс, обусловленный лимитом Хейфлика. Лимит Хейфлика — всего лишь следствие, наведённое эпигенезом. Сенесцент обуславливает сенилит, и наоборот: сенилит ⟺ сенесцент. Непрерывное провоспаление и форсаж их выводит работу клеток организма (клетки-обслуги и стем-клетки) за пределы оптимума, то есть не в оптимальном режиме функционирования гомеостаза, что повышает их резистентность, но снижает толерантность. В итоге эффективность, функциональная производительность, Жизненная Сила таких клеток значительно падает, так как они находятся в состоянии УКАМ* (Универсальный Клеточный Адаптационный Модус), в стадии стабилизированной модификации истощения. Сенесцент — это и есть модификация УКАМ с переходом в устойчивую невозвратную фазу истощения. Стабилизацию модификатам придаёт эпигенез*.
Онкологическая модификация является разновидностью сенесцента, противоположным крылом одного механизма [25]. Сенесцент и онкология — это две крайности одного и того же процесса, спровоцированного гипоксией и реализованного через HIF-1 и NF-κB.
Значение HIF – как детектора-модератора уровня кислорода в клетках. Если внутри клетки кислорода много, то HIF-белки разрушаются. По сути, HIF это буквально ключ от нашей молодости, так как поддерживает кислородную энергетику. Как только уровень кислорода снижается, какая-то часть этого белка поступает в ядро клетки и стимулирует транскрипцию генов, отвечающих за обновление и модификацию этой клетки. То есть в норме HIF противодействует гликолизу, но не в случае негипоксической гипоксии при сенесценте и онкологии. При сенесценте происходит энергетическая депрессия (митохондриальная недостаточность), которая и является причиной негипоксической гипоксии, поэтому HIF здесь не срабатывает по причине эпигенеза и резистентности генома. Негипоксическая гипоксия может провоцировать как оксидативный стресс в митохондриях (отпечаток на эпигеноме в виде смены эпигеномных паттернов), так и другие внешние факторы индукторы сенесцента. Методы активации, стимулирования HIF в этом случае малоэффективны, так как изменения произошли не на функциональном уровне клетки, а на структурном, на уровне паттернов эпигенома (анизо-паттерны*). Паттерны – элементы гистоновой рубашки в норме отвечающие за геномные блоки или экспрессии. При онкологии и сенесценте происходят смещения паттернов, что ведёт к экспрессированию паттерна регулировки торможения (расторможения) репликаций. Таким образом, сенесцентные клетки перемодифицированы через механизмы эпигенеза на гликолиз, что проявляется в виде негипоксической гипоксии и невозможности клетки к высшим дифференциальным функциям.
При онкологии тоже запускаются мощно эндогенные механизмы провоспаления с подключением триггерных программ разрегулировки репликаций.
Сенесцент зарождается среди модифицированных ювентальных* иммунных клеток
Путь к сенесценту проходит через появление из ювентальных клеточных линий новых клеточных устойчивых, невозвратных иммунных модификатов M1, M2, Th1, Th2, Th17… Причём автор считает, что правильнее выделять возвратные (временные, зависящие от внешних условий) активированные фенотипы и устойчивые сенесцентные (независимые от внешних условий) модификаты. Возврата в исходное состояние нормы у них нет, так как это связано не только с эпигенетическими закрепляющими их статус перестройками (перекос процессов метилирования и ацетилирования на гистоновой мантии хроматина), но и с закрепляющими их статус на уровне сенилита.
Макрофаги, ассоциированные со старением
Изучение проблемы «сенолитиков» показало, что сенесцентные клетки (СК) несут на себе один из маркёров сенесцентности р16, но не все р16+ клетки являются сенесцентными. Большую их часть составляют клетки иммунной системы (ювентальные), ответственные за удаление СК (сенесцентных клеток). Таким образом, с возрастом происходит не только накопление СК, но и нарушение работы иммунной системы, способной в молодом возрасте самостоятельно удалять СК за счёт доминирования ювентальных клеток (ЮК), которые подавляют сенесцентные клетки, а последние и являются источником выделения факторов воспаления, а также SASP*. Основными «действующими лицами» такой перестройки оказались макрофаги, ассоциированные со старением, которые, как оказалось, обладают многими свойствами СК.
Эпигенетическая суть сенесцента
Эпигенез — это когда процессы развития клеток регулируются не сигналингами, идущими из вне или изнутри и действующие на прямую на геном, а опосредовано через эпигеном. Согласно эпигенетической теории, генные программы могут корректироваться не сигнальными молекулами, а благодаря белкам, которые обслуживают ДНК. Эти белки гистоны, из которых образуются гистоновые рубашки, не только защищают ДНК или участвуют в починке нарушенных участков спирали, но и при смене облика гистоновой рубашки менять экспрессируемость генов. Смена гистоновой мантии (метилирование – ацетилирование) меняет статус ДНК. Перестройки в этой мантии зависят от множества различных факторов (внутренних и внешних) и могут создать множество вариантов эпигенетических перекроев в этой мантии, а это в свою очередь может вызвать множество инвариантов изменений или коррекции в экспрессии тех или иных программ. Сенесцент является одним из инвариантов такого эпигенеза, результатом которого клетка снижает свою энергетику в митохондриях, а затем перестраивается на ограниченную возможность к репликациям из-за подавления механизма митозов на этапе G1 клеточного цикла. При этом особенность сенесцентирования клеток в том, что это направляемый процесс и регулируемый извне, с верхних этажей становления организма. Только в самом начале первичный сенесцент в тимусе зарождается изнутри согласно программам морфогенеза, а затем он регулируется только через эпигенез. В свою очередь сенесцент это наведённый извне процесс и зависит от статуса на общеорганизменном уровне, в том числе и сенилита. Одно определяет другое.
Причём запуск сенесцента запускается не сразу, а через замедление репликаций в последующих потомствах клеток. В этих потомствх происходит укорочение теломеразы, что доходит в конечном итоге до критического рубежа – полной остановки репликаций. С этим связано медленное проявление процесса, он может начаться ещё в ранней юности или детстве, но быть проявленным через десятилетия.
Согласно теории Хейфлика сенесцент заложен изначально в программу клеток, что показали эксперименты над ювентальными фибробластами, и обеспечивает около 52 репликаций дочерних клеток, что зависит от степени укорочения теломер. Но длина теломер и скорость её укорочения часто не коррелирует с долгожительством. Активность фермента теломераза, который регулирует восстановление теломеры, чаще совпадает со статусом ювентальности.
Согласно теории Гарбузова сенесцент это наведённый (но изначально управляемый, коммитированный, предусмотренный) процесс и через него регулируются этапы онтогенеза на уровне эпигенома. Клетки любой ткани имеют изначальные предписания реагировать на некоторые условия неспецифически, путём сенесцента. Таким образом, сенесцент это программа неспецифического ответа, реагирования на самые различные факторы, в том числе и клеточный оксидативный стресс и др., а также на ряд определённых изменений в организме. При этом всегда подавляется клеточная энергетика (энергетическая депрессия), статус которой закрепляется на эпигеноме. Сенилит и другие условия дискомфорта и дисбалансов создают единый неспецифический ответ, наводящий на сенесцент. Долгоживущие животные (землекопы – 37 лет) и короткоживущие (мыши 2 – 3 года) имеют такую разную Онтодианную Линию Жизни не из-за особенностей их клеток, а благодаря проработкам иммунных механизмов в верховных «штабах» регулировок. Эти штабы на верхних этажах более высоко и тонко проработаны. Другими словами, степень иммунной реювентализации у них намного выше, что часто сочетается с более высокой и длительной степенью сохранения реювенилизации.
От чего зависит степень сенесцента ткани? Она зависит не от числа репликаций, через которые проходят её клетки, а от численности сенесцентных клеток, их доминирования над ювентальными и величиной вала производства SASP*. Число очередных сенесцентных клеток в ткани постоянно нарастает из-за очередных волн интервенциализации процесса.
Сенесцент — это нарушение геномной транскрипции и экспрессии генов, но не через генопрограммы, а через эпигенез
В частности, гиперэкспрессируются HIF-1 (гены, регулирующие гипоксию), а триггером идёт NF-κB (транскрипционный фактор относят к эндогенным промоторам, отвечает за провоспаление), что ведёт к дисфункции аутофагии (ATG*). Как результат ослабляются репарация, реювентализация клеток.
Такие перестройки всегда идут в ущерб основным клеткам-«офицерам», или стем-клеткам. Энергетические и трофические возможности в них ухудшаются, вся клеточная система ткани приближается к гликолизному существованию. Затем они тоже вырождаются, появляются устойчивые трансформаты* (в отличие от модификатов, процесс переходит на стем-клетки) с последующими дегенеративными процессами. Возможно, их правильнее называть редуктантами, так как здесь происходит замена стволовых высокофункциональных клеток на клетки с низким функциональным потенциалом. Связано это с входом в зону гликолизного существования. Гликолизность стем-клеткам передаётся от иммунных клеток (макрофаги…).
В клетках-трансформатах и модификатах подавлены системы аутофагии и реювентализации, что не допускает полное самовосстановление. Это и является основой для устойчивого проявления репликативного торможения, функциональной недостаточности, включая митохондриальную, шлейфом идут оксидативные стрессы, страдает ретикулярно-рибосомальная сеть с нарушением производства протеома и ювентального UASP, появлением избытка БТШ (белки теплового шока), а также внешнего сенесцентного секретома (SASP)… Через свой сенесцентный секретом эти клетки продолжают переактивировать окружающие клетки, переподчиняя их себе.
В этом SASP секретоме избыточно находятся и молочная кислота (лактат), перекиси и другие выделения гликолиза (метаболом)… С ними связано появление чувства хронической усталости, немощности… Образуется замкнутый порочный круг: сенилит активирует сенесцент, а сенесцент индуцирует сенилит. Они взаимозависимы, и при прогрессии одного активируется и другое. Механизмы гомойототопии мы устранить не можем, но компенсировать её негативную сторону можно ускорением механизмов ювентализации. Увеличение количества сенесцентных клеток приводит к их доминантности над ювентальными*. Таким образом происходит погашение (не угасание, а навязанное гашение) функциональности в большинстве тканей организма. Как результат — появление огромного поля возможностей (которое только расширяется из-за сенесцента) для проявления самых различных анизомалий*, чего не было в юности. Появившиеся проблемы как на клеточном уровне, так и на общеорганизменном сокращают онтодианную линию жизни* организма, определяют ей финальный предел. Эта линия жизни определяет так называемую адаптированную смертность для каждого вида (самоуничтожение, феноптоз). Формируется четко выраженный сенилитный фенотип организма, который только наращивает свой потенциал. На определённом рубеже сенесцентность и сенилит становятся доминирующими и подводят организм под итоговую черту — мортальный исход.
Реализация модификации и сенесцента макрофагов через гликолиз и метаболическое перепрограммирование [26]
Специфические метаболические пути в макрофагах тесно связаны с их фенотипом и функциями. Провоспалительные макрофаги (M1) полагаются в основном на гликолиз и демонстрируют нарушение цикла трикарбоновых кислот (ЦТК) и митохондриального окислительного фосфорилирования (ОФ), в то время как противовоспалительные макрофаги (M2) в большей степени зависят от митохондриального ОФ.
Модификация связана с гликолизом. Но там, где гликолиз, — там гипоксия (HIF-1) и провоспаление (NF-κB) иммунных клеток. Однако это не настоящая гипоксия, а так называемая негипоксическая гипоксия, то есть вокруг клеток кислорода достаточно, но они к нему нечувствительны. Аналогичный тип негипоксической гипоксии наблюдается и при онкологии, но порог глубины гипоксии здесь намного выше, и поэтому вовлекаются триггерно по эпигенетическим механизмам и другие механизмы, включая пролиферативные. Однако стем-клетки, или клетки-функционеры, не выдерживают длительно гипоксию, им нужен высокий потенциал ОФ. А макрофаги-модификаты не обеспечивают их нужным. Естественно, в главных функциональных клетках происходит ослабление их функционального состояния, Жизненной Силы, или они вырождаются. Тогда как в онкологических клетках происходит репликационная трансформация, частые репликации помогают им выжить.
Тканевые макрофаги образуются в процессе эмбрионального развития и из циркулирующих моноцитов. Макрофаги обладают особыми метаболическими характеристиками, которые коррелируют с их функциональным состоянием, известным как метаболическое перепрограммирование. Показано, что макрофаги с повышенным провоспалением повышают и уровень гликолиза. Гликолитическая активность имеет решающее значение для функции макрофагов.
Метаболическая сигнатура макрофагов M2 сильно отличается от сигнатуры макрофагов M1. Макрофаги M2 не демонстрируют повышенного гликолиза. Но показано, что гликолиз играет роль в начальной активации M2-макрофагов.
Автор считает, что первичные базовые механизмы сенесцента и ракового перерождения схожи, а рак является крайностью сенесцента. Также считает, что методы лечения рака отчасти совпадают с методами борьбы с сенесцентом [27].
Энергетические проблемы у сенесцентных макрофагов или Митохондриальная недостаточность
Ранее автор обсуждал подробно связь сенесцентных (стареющих) и раковых клеток. Помимо всего другого, общим у них является митохондриальная дисфункция, энергетическая депрессия и переход на гликолизный метаболизм. Оба эти процесса являются эпигенетически зависимыми и по сути это проявление двух крайностей одного и того же процесса, связанного с регулировкой репликаций (делений – митозов клеток). В одном случае – это ограничение, а в другом – полная неуправляемость репликациями. В первом случае нарушены транспозитные рычаги регулировок митозов, а в другом – контрпозитные. Но во всех этих случаях это очевидно обусловлено невозможностью клетки в той или иной степени полноценно реализовывать свои энергетически-зависимые обязанности из-за простого дефицита энергии.
Важно подметить, что стволовые раковые клетки воздействуют на подавление иммунных клеток (макрофагов) путём провоцирования в них сенесцента (старения, что делает их беспомощными в войне с онкоклетками). Старые иммунные клетки не активны, бессильны, теряют способность к пролиферациям и самовосстановлению. Также раковые опухоли способны вырабатывать провоспалительные цитокины (интерлейкин-6, IL-6), стимулируя сами себя. Интерлейкин-6 участвует в развитии злокачественных опухолей, в процессах инвазии и метастазирования. Он может стимулировать пролиферацию, выживание, метастазирование и инвазию опухолевых клеток.
Но с другой стороны этот же интерлейкин-6 является основным провоспалительным цитокином и у сенесценных клеток! В обоих случаях создаётся очаг воспаления. То есть, казалось бы, два разных процесса регулируются одним и тем же сигналинговым медиатором. Не означает ли это, что у раковых клеток один и тот же состав SASP (метаболический выброс), как и у сенесцентных клеток, но только более сильный?
Кроме того, в отличие от здоровых клеток, сенесцентные клетки выделяют в окружающую среду ряд промежуточных продуктов метаболизма, в том числе лактат, пируват, аланин. Раковые клетки тоже выделяют в окружающую среду промежуточные продукты метаболизма, в том числе лактат, пируват и аланин из-за гликолизного эффекта Варбурга.
Это указывает, что чтобы заставить иммунитет бороться со старческими и онкологическими клетками его надо в обоих случаях омолаживать, переводить в статус ювентальности. В помощь этому могли бы быть гормон роста, метформин, дегидроэпиандростерон и витамин D.
Эту концепцию подтверждают и данные, что такое вещество как никотинамидмононуклеотид (NMN), которое участвует в производстве АТФ (энергетической валюте) и улучшает функцию митохондрий, может оказывать положительное действие как при сенесценте клеток, так и при раковых. При этом продлевает жизнь животным с онкологией. Известно, что NMN способствует повышению уровня NAD+ в организме, замедлению процессов клеточного старения, увеличению продолжительности и повышению качества жизни. Улучшение энергетики митохондрий, ослабляет эпигенетические изменения, проявляемые при сенесценте и раке.
В свою очередь NAD+ связан с сиртуинами, которые считают факторами молодости. Они главные препараты для anti-age медицины, а точнее – разные активаторы синтеза сиртуинов и синтеза NAD+. А что такое NAD+? Молекула важнейший активатор метаболизма, энергетики и клеточного кислородного дыхания (не говоря уже о сотнях других важнейших биохимических реакций).
Введение того же NMN в экспериментах на мышах, которым были привиты раковые стволовые клетки, приводило к размножению нестареющих макрофагов (ювентальных) и уменьшению иммуносупрессивных факторов, вырабатываемых стареющими макрофагами, что в итоге предотвращало рост опухоли и приводило к увеличению продолжительности жизни мышей. (Кстати, попутно отмечу, что NMN как помогает сохранять ювентальность, так и противодействует раковым клеткам, что отрицает бытующее мнение, что сенесцентные клетки тормозят проявление раковых клеток).
Таким образом, NMN не просто содействует кислородной энергетике раковых и сенесцентных клеток, но и их обратной ремодификации в нормальные! Конечно, это как самостоятельный метод не решит всю глубину проблемы реонкологизации раковых клеток или реювентализации сенесцентных, но в Комплексных Программах значительно повысит их эффективность и, возможно, станет решающим действием. Если NMN решает вопрос нормализации энергетики клеток, то другие методы как ДХА [28], препараты Mg, Куркумин-Адванс, Витамин D3 и др. помогают устранить провоспалительный статус, запуск механизмов апоптоза больных клеток и др. Совместное сочетание значительно усилит общий положительный эффект.
Поэтому важным компонентом является подключение и Никотинамидмононуклеотид.
Как итог, можно утверждать, что целью является усиление доминантности ювентальности. В этом плане интерес представляют сенолитики. Но, тем не менее, потенциал их возможностей тоже ограничен.
Какова роль реципрокного механизма регулировок баланса ювентальных и сенесцентных клеток и что общего его с механизмом автоколебательного контура в регулировке NMN?
Степень возрастной (или онтофизисной*) зрелости ткани зависит от доминантного соотношения ювентальных и сенесцентных клеток. Причём у каждого крыла этого статуса имеются свои собственные механизмы авторегулировок, а взаимоотношения этих крыльев регулируется через механизм автоколебательного контура. Движущими силами здесь являются транспозитные и контрпозитные механизмы.
Для наглядности проанализируем как регулируется уровень NAD+ (НАД+) в клетке и может ли он определять тип метаболизма клетки: гликолизного или кислородного (окислительного фосфорилирования, ОФ). Известно, что НАД участвует в метаболизме как гликолиза, так и окислительного фосфорилирования. Однако он не участвует в регулировке Окислительного Фосфорилирования, но НАДН, образовавшийся в процессе гликолиза, в норме является «стартером», который обеспечивает энергию для синтеза АТФ в митохондриях. Недостаток НАД в гликолизе не обеспечивает окислительное фосфорилирование.
Переход от аэробного гликолиза к окислительному фосфорилированию и наоборот регулируется следующим образом:
При наличии кислорода НАДH может отдавать свои электроны в электрон-транспортную цепь, возвращаясь в форму НАД+, пригодную для использования в гликолизе. В качестве бонуса при этом образуются ещё несколько молекул АТФ.
Сенесцентные клетки (также, как и онкологические) переходят на метаболизм гликолиза (аэробный гликолиз = псевдогликолиз) из-за нарушения работы митохондрий. Переход к гликолизу связан с тем, что большое число нефункциональных митохондрий не может обеспечить необходимый уровень продукции АТФ.
Механизм сенесцентности
- Снижение интенсивности окислительного фосфорилирования из-за нарушения митохондриальной динамики.
- Усиление гликолиза — это происходит с помощью аллостерической регуляции уже наработанных ферментов гликолиза или повышения экспрессии генов, кодирующих ферменты гликолиза.
- Регенерация NAD+ — преимущественно путём превращения пирувата в лактат, что ведёт к интенсивной секреции лактата.
Механизм рака
Раковые клетки (клетки злокачественных опухолей) активно используют метаболизм гликолиза (эффект Варбурга) из-за особенностей энергетического метаболизма, характерных для активно растущих клеток. В отличие от нормальных клеток, у которых основным способом синтеза АТФ является окислительное фосфорилирование, у большинства раковых клеток повышен уровень гликолиза.
Причины
- Адаптация к гипоксии. В условиях пониженной оксигенации опухолевые клетки не способны к запуску реакций окислительного фосфорилирования, что вынуждает их переходить на гликолиз.
- Высокая потребность в синтезе макромолекул для активного роста. В результате гликолиза образуются мономеры, необходимые для синтеза нуклеиновых кислот, белков и липидов.
- Компенсирующая адаптация, связанная с дисфункцией митохондрий. Усиленный гликолиз рассматривают как компенсирующий механизм, связанный с нарушениями функций митохондрий. Однако гликолиз не является универсальным признаком всех опухолевых клеток — некоторые опухолевые линии способны обратимо переключаться между гликолизом и окислительным фосфорилированием в зависимости от наличия глюкозы в среде.
Последствия
- Обеспечение энергией — гликолиз генерирует АТФ быстрее, чем окислительное фосфорилирование, что даёт селективное преимущество в быстро растущих опухолевых клетках.
- Стимуляция роста — высокая скорость гликолиза способствует росту опухолевых клеток через повышение образования предшественников для синтеза липидов, нуклеотидов и аминокислот.
- Закисление внеклеточного пространства — метаболические продукты гликолиза (лактат и протоны) вызывают закисление, что способствует инвазии и метастазированию раковых клеток.
Гены, регулирующие синтез сиртуинов и НАД, впервые обнаруживаются у примитивнейших форм жизни. Например, у вирусов вибриофагов. Причём уровень их циклически меняется, колеблется в виде биоритмов то в большую, то в меньшую сторону и зависит от многих факторов, в том числе и от времени суток, стресса, уровня пищевых субстратов… Напомню, что НАД это важнейший активатор метаболизма и клеточного дыхания. Соответственно, как только запускается активная фаза биоритмов, потребность в НАД резко возрастает, для чего и активируется фермент никотинамид-фосфорибозилтрансфераза (НАМФТ), запускающий синтез НАД. Концентрация НАД начинает расти, стимулируя метаболизм и разные процессы активной жизнедеятельности, нуждающиеся в НАД, среди которых есть и… сиртуины. Именно сиртуинам для выполнения своих функций нужно очень много НАД. (НАД-сиртуиновый коктейль и является сегодня главным anti-age препаратом). Важно что НАД активирует сиртуины, а те в свою очередь начинают блокировать центральный фактор (BMAL1:CLOCK) в системе регуляции биоритмов, что в свою очередь блокирует активность фермента НАМФТ. Ведь, напомню, что сиртуины есть не что иное, как блокаторы многих генов. Снижение же активности фермента НАМФТ закономерно приводит к снижению синтеза НАД, что влечет за собой падение активности метаболизма, то есть неактивную фазу любых биоритмов. А поскольку для работы сиртуинов необходим НАД, через некоторое время активность сиртуинов тоже начинает снижаться. Вследствие этого блокада гена, отвечающего за активность фермента НАМФТ, постепенно ослабевает, и его синтез возобновляется, что знаменует собой активную фазу биоритмов. И далее опять по кругу – то есть сугубо принцип регулировок автоколебательного контура. По этому же принципу идёт регулировка баланса ювентальных и сенесцентных клеток. Если бы этот оптимальный баланс был устойчивый, то ткань могла бы сохранять свой статус юности неограниченно. Но, тем не менее, этот баланс постоянно сдвигается за счёт механизмов гормезисореза*, что движет организм вдоль Онтодианной Линии Жизни.
Итак, сиртуины созданы для регуляции биоритмов. Очевидно, что через эти же сиртуины может регулироваться и метаболический баланс взаимоотношения гликолиз/аэробность. Любая сенесцентная или онкологическая клетка меняет этот баланс в пользу гликолизу, то есть перенастраивается. В этом случае регулируется весь самый большой цикл биоритма – онтогенетический. Только в отличие от малых циклов, биоритмов (например, циркадный – суточный) большой цикл не имеет механизмов возвратности в исходное состояние. Этому мешает блокировка степени потентности стволовых клеток еще в период эмбриональности. Высшие организмы теряют способность к регенерации и полного самоомоложения, то есть поворачивать балансы ювентальных и сенесцентных клеток в пользу ювентальных. Именно отсутствие механизма возвратности в исходное состояние (самоомоложения) ведёт к накоплению возрастных изменений в тканях, что проявляется в физиологическом статусе их онтофизиса* и воплощается через новые фенотипы.
Единство генных механизмов сенесцента и онкологии
Автор [25] проанализировал и показал, что возрастная онкология (как проявление канцерогенезного типа анизомалии) является крайним проявлением сенесцента, а генные механизмы, обеспечивающие их становление, практически совпадают. Канцерогенез — это один из видов неизбежных анизомалий, обеспечиваемых всем ходом сенилитных и сенесцентных перестроек (гормональных, иммунных, провоспалительных…) и становящихся одним из механизмов мортуса* (мортального исхода). Неминуемые сенилитные и сенесцентные перестройки являются базой для канцерогенеза.
Важно то, что показания у лютеолина и мелатонина в отношении сенесцента, сенилита и онкологии совпадают.
Эту концепцию подтверждают и данные, что такое вещество как никотинамидмононуклеотид (NMN), которое участвует в производстве АТФ (энергетической валюте) и улучшает функцию митохондрий, может оказывать положительное действие как при сенесценте клеток, так и при раковых. При этом продлевает жизнь животным с онкологией. Известно, что NMN способствует повышению уровня NAD+ в организме, замедлению процессов клеточного старения, увеличению продолжительности и повышению качества жизни. Улучшение энергетики митохондрий, ослабляет эпигенетические изменения, проявляемые при сенесценте и раке.
Также эту идею подтверждают данные о том, что Klotho препятствует клеточному старению (сенесценту), апоптозу, воспалению, иммунной дисфункции, фиброзу и неоплазии. Делает это он через подавление четырёх сигнальных путей, которые по-разному связаны со старением: трансформирующий фактор роста β (TGF-β), инсулиноподобный фактор роста 1 (IGF-1), Wnt и NF-κB. Очевидно они находятся в числе тех генов, которые находятся в контрпозициях в пределах одного и того же маятникового механизма регулировок, удерживающего толи гомеостаз ювентальности, толи сдвигающие его в сторону сенесцента.
Антивозрастной белок Клото как новый потенциальный супрессор опухолевого роста. Эта его способность привлекает особое внимание.
Данные по Клото также подтверждает концепцию автора, что сенесцент и онкологизация клеток имеют общие механизмы и являются двумя крайностями, противоположными рычагами единой системы регулировок пролифераций (единого гомеостаза). Этот механизм балансировки-регулировки скорости пролифераций выходит за рамки оптимума (гомеостаза) и становится не управляемым (анизостаз), при этом появляются новые клеточные фенотипы. Клото действует как на онко, так и на сенесцентные клетки, что указывает на их общие начала. На определённом этапе Клото теряет силу восстановления динамики процесса, так как накапливающиеся процессы эпигенеза пересиливают его возможности. Нормальная регулировка этого гомеостаза блокируется уже на уровне эпигенома, а не на уровне генов. Известные генные онкосдвиги являются вторичным проявлением эпигенеза. До сих пор преобладает мнение, что сенесцент важен для остановки онкологизации, но это неверно, так как в обоих случаях идёт провоспаление, гликолиз (фундамент без которого невозможно проявление онкологии), а добавление ряда триггерных факторов-провокаторов на этом фоне только усиливает вероятность вспышки раковой трансформации. Эта специфичность-неспецифичность факторов определяет различия в динамике эпигеномных перестроек, что ведёт к затрагиванию разных рычагов одного и того же маятникового механизма и вызывает два разных типа анизостаза* (онко и сенесцент).
Единство энергетической стороны обеспечения клеток у онко и сенесцентных клеток
Причём сенесцент неспецифичен (основан на клеточных механизмах УКАМ* - универсальный клеточный адаптационный модус) и подобен неспецифичной ОАС*, (регулируется гормонами и медиаторном на общеорганизменном уровне), тогда как для онко нужны специфичные провокаторы (триггеры), которые тем не менее более глубоко затрагивают механизмы УКАМ. Таковыми являются механизмы регулировок систем энергетики и пролиферации клеток. В зависимости от того в какую сторону произойдёт крен того или иного рычага маятника происходит появление новых фенотипов клеток в виде сенесцента или онко.
Klotho, как наблюдается в нескольких опухолях, индуцирует апоптоз клеток и ингибирует рост опухоли путём ингибирования передачи сигналов инсулина/IGF-1 за счёт ингибирования фосфорилирования тирозина рецептора... Известно, что биоактивность свободного инсулинового фактора роста 1 (IGF-1) увеличивает скорость оборота опухоли. В тоже время тот же IGF-1 проявляет способность к увеличению накопления сенесцентных клеток.
Тем не менее, у людей результаты исследований противоречивы. Например, есть доказательства существования «двухфазной» (U-образной) взаимосвязи между уровнями IGF-1 и продолжительностью жизни: как высокий, так и низкий уровень IGF-1 увеличивал смертность от возраст-ассоциированных заболеваний у мышей. Также есть информация, что снижение уровней IGF-1 в пожилом возрасте может способствовать ускоренному старению за счёт усиления митохондриальной дисфункции, выработки окислительных радикалов. Достаточная концентрация IGF-1, в свою очередь, препятствует образованию свободных радикалов, предотвращает окислительное повреждение в митохондриях.
Это подсказывает, что сенесцент и онкология сопряжены с механизмами энергетики клетки и перевода её в анаэробный и провоспалительный статус, осуществляя это через механизмы регулировки утилизации глюкозы. Следовательно, эти механизмы регулировок — это ключ
Чтобы заставить иммунитет бороться со старческими и онкологическими клетками его надо в обоих случаях омолаживать, переводить в статус ювентальности.
Важно подметить, что стволовые раковые клетки воздействуют на подавление иммунных клеток (макрофагов) путём провоцирования в них сенесцента (старения, что делает их беспомощными в войне с онкоклетками).
Онкологическая модификация является разновидностью сенесцента, противоположным крылом одного механизма [25]. Сенесцент и онкология — это две крайности одного и того же процесса, спровоцированного гипоксией и реализованного через HIF-1 и NF-κB.
Модификация связана с гликолизом. Но там, где гликолиз, — там гипоксия (HIF-1) и провоспаление (NF-κB) иммунных клеток. Однако это не настоящая гипоксия, а так называемая негипоксическая гипоксия, то есть вокруг клеток кислорода достаточно, но они к нему нечувствительны. Аналогичный тип негипоксической гипоксии наблюдается и при онкологии, но порог глубины гипоксии здесь намного выше, и поэтому вовлекаются триггерно по эпигенетическим механизмам и другие механизмы, включая пролиферативные. Однако стем-клетки, или клетки-функционеры, не выдерживают длительно гипоксию, им нужен высокий потенциал ОФ. А макрофаги-модификаты не обеспечивают их нужным. Естественно, в главных функциональных клетках происходит ослабление их функционального состояния, Жизненной Силы, или они вырождаются. Тогда как в онкологических клетках происходит репликационная трансформация, частые репликации помогают им выжить.
При онкологии тоже запускаются мощно эндогенные механизмы провоспаления с подключением триггерных программ разрегулировки репликаций.
Что такое митохондриальные модификации? И почему они вектор-причина нормального (ювентального) или онкологического, или сенесцентного пути развития клеток?
Паттерны – элементы гистоновой рубашки генома, в норме отвечающие за геномные блоки или экспрессии. При онкологии и сенесценте происходят смещения паттернов, что ведёт к экспрессированию паттерна регулировки торможения (расторможения) репликаций. Таким образом, сенесцентные клетки перемодифицированы через механизмы эпигенеза на гликолиз, что проявляется в виде негипоксической гипоксии и невозможности клетки к высшим дифференциальным функциям.
Митохондриальная природа эпигенеза и какая связь их с эпигенетическими паттернами. Эпигенетические паттерны связаны с метилированием ДНК и ацетилированием гистонов — двумя основными механизмами регуляции экспрессии-репрессии генов, которые не связаны с изменением первичной последовательности ДНК. При этом метилирование подавляет активность генов. Ацетилирование гистонов нейтрализует положительный заряд гистонов, что ослабляет их хватку в ДНК, а точнее гистон диссоциирует (отдалится от ДНК), и упаковка ДНК станет более «рыхлой» (менее плотной). Тогда белки-регуляторы (факторы транскрипции) смогут легче получать доступ к генам. Ацетилирование делает гистоновую рубашку «проницаемой» не повсеместно, а только на том участке где осуществляется функция транскрипции. За пределами этой транскрипции это ацетилирование не срабатывает. Оно целевое. Это способствует экспрессии генов. Ацетилирование обнаруживается в области генов, на которых активно идёт транскрипция. Увеличение уровня метилирования ДНК обычно сопряжено со снижением уровня ацетилирования гистонов. Но это в норме, а при эпигенетических сдвигах эта норма нарушается. Тогда генами начинает управлять не баланс нормо-гистоново-ацетилированной рубашки (соответствует настройкам для ювентальности), а статус метилома в нарушенной рубашке. Это подобно тому как маленький размер рубашки не даёт возможности двигаться рукам.
Откуда исходят первичные механизмы реализации сенесцента: со стороны искажения энергетики в митохондриях или со стороны эпинарушений? Активность энергетики митохондрий сопряжена с эпигеномом, между ними реципрокная (взаимозависимая) авторегулировка, когда статус каждого из этих процессов зависит жёстко от противоположного. Это единая система, в которой нет главенства верхнего и нижнего этажа, а поэтому не имеет значения где первично произошли изменения, так как они обязательно отразятся и на другом крыле маятника и в любом случае будут исходить сигналы на сенесцент. Будь то нарушение энергетики митохондрий или эпигенез – всё это ослабит автоколебательный потенциал во всём контуре, и вся система станет резистентной (нечувствительной). Это и есть анизостаз* – выход из оптимальных рамок данного гомеостаза. Изначально они отрегулированы на оптимум во взаимоотношениях. И каждая из сторон стремится вернуть систему в исходное состояние, имея для этого свои собственные механизмы. Каждое отклонение за пределы гомеостаза в системе ведёт к регулирующим коррекциям с противоположной стороны, и система возвращается в исходное положение. Эпигеном – регулятор гомеостаза. Если геном отвечает за морфогенез, то эпигеном – за онтофизис*, модификаты, фенотипы и онтогенез. Эпигеному предназначена роль балансира, регулировщика постоянства: если какая-либо функция, например энергетики или другая, у клетки начинает зашкаливать и находится в экстренной ситуации, не поддаётся регулировке на генном уровне, то начинают вырабатываться вещества, которые меняют среду (заряды + – или «защелачивание» «закисление», или…) и перестраивают, переводят эпигеномный маятник в обратную сторону: вместо метилирования происходит ацетилирование (доступ к генам и их экспрессия) или наоборот (гены блокируются), а процесс идёт до тех пор пока система не уравновесится и не придёт в исходное состояние. Блокировка (разблокировка) идёт не в отдельных генах, а в целых блоках. Именно для этого предназначен эпигеномный балансир, который находится не где-то в клетке, а напрямую на геноме и регулирует активность его.
Эпигеном как зона восприятия влияния на геном. Но на эпигеномный балансир могут влиять многочисленный факторы, в том числе и гормональный фон, иммунный фон, оксидативный или иные типы клеточных стрессов... Через них может предусматриваться регулировка становления модификатов, фенотипов, сенесцента, онтофизиса и… вплоть до сенилита.
Исказить нормо-гистоновую рубашку могут многие факторы, но в первую очередь те, которые связанные с изменением энергетики и уровнем провоспаления. Они изменяют электростатические заряды и тем самым позволяют пройти процессам «перекройки» рубашки. Ацетилирование и метилирование несут разный электрозаряд, где ацетилирование приводит к нейтрализации положительно заряженных гистонов, а значит смещение динамики в пользу ацетилирования может произойти в результате смены электрозарядов вокруг хроматина. К смене зарядов могут привести даже банальные метаболические перекосы, когда вырабатываются иные ионы. Очевидно все эти перекосы в первую очередь отражаются на иммунных клетках – макрофагах-резидентах, отвечающих за трофику функциональных клеток.
Известно, что сенесцент сопряжён с митохондриальной недостаточностью (МН), дисфункцией. В свою очередь эпигенез сопряжен с МН. Это позволяет утверждать об митохондриальной связи эпигенеза. Эпигенез вторичен и особенности его разнообразных проявлений зависят от той или иной степени активности митохондрий. В любом случае эпигенез «консервирует» новый статус МН.
Кроме того, эпигенез повторяет (отражает) на себе морфогенез, что позволяет сигналинговым молекулам ориентироваться на хроматине.
Что такое ювентальные клетки, ювентальный реверс и можно ли перевести сенесцентные клетки в ювентальные?
В первую очередь статус ювентальных клеток противоположен сенесцентным, которые происходят из первичных девственных юных клеток.
Ювентальность, ювентальные клетки — состояние молодости, относящееся сугубо к клеточному уровню. Термин введен с целью различения от понятия ювенильность, то есть молодости всего организма на основе особого иммунного статуса и гормонального фона. Механизмы реализации этих процессов разные и происходят на разных уровнях. Ювентальные клетки не имеют блокировки ряда генов, что присуще сенесценту, или точнее, сенесцентные клетки блокируют гены ювентальности. Речь идёт об антисенесцентных генах (антисенесценция) и о генах ювентальности и сенесцента (коммитирующих генах). Это следует понимать, что одна группа транспозитных генов противодействует сенесценту, а другая группа контрпозитных генов содействует сенесценту. Таким образом взаимодействие этих генов создаёт своеобразный маятниковый механизм регулировки, в котором доминирование того или иного крыла ведёт к тому или иному статусу (фенотипу) клетки.
При этом ювентальные клетки* обладают ювентальными эпигенетическими паттернами, тогда как у сенесцентных клеток эти паттерны сенесцентные, а у онкологических – свои онкологические паттерны – свои гистоновые надстройки. Ювентальные клетки имеют изначальную экспрессию ювенильных генов, что уравновешивается = отображается на их эпигеноме (ювентальные паттерны), который тоже соответствует ювенильности, в итоге это равновесие генома и эпигенома. По ряду причин эпигенез будет в дальнейшем искажать транскрипцию генома и ослаблять реализацию его возможностей. Эпигеном будет менять потенциал генома!
Как это регулируется до конца неизвестно, но ясно что осуществляется это через сдвиг баланса метилирования и ацетилирования на гистоновой рубашке.
Возможная роль уровня фосфатов в регулировке сдвига эпигенома = эпигенеза. Причём можно предполагать, что этот сдвиг связан с ослаблением энергетики клетки (митохондриальная недостаточность), что в свою очередь снижает потребность в «стройматериале» – утилизации фосфатов и фосфолипидов (фосфатидилхолин, то есть холин). Причём именно они несут отрицательный заряд, а накопление этих фосфатов поляризует субстрат внутри ядра клетки. Особенность молодых клеток (ювентальных) в том, что они содержат значительно выше уровни этих молекул с отрицательным зарядом, который способен легко гасить радикалы и активные формы кислорода, являющиеся в больших количествах топливом для оксидативного стресса. Эта обратная поляризация может стать фактором для смены баланса метилирование/ацетилирование. А это одно из важнейших условий нужных для эпигенеза – смены качества эпигеномной рубашки. Таким образом, во взаимодействии генома-эпигенома значение имеет и уровень насыщенности раствора фосфатами, которые имеют отрицательный заряд. Кроме того, это не означает что этот отрицательный заряд можно заменить, например, другими ионами или анионами водорода, которые имеют отрицательный заряд. Отрицательный заряд фосфатов имеет специфическую каталитическую направленность действия, которую невозможно заменить. Он направлен как на поддержание синтеза ДНК, так и на создание фосфолипидных мембран, и на…
Так выявлен механизм, когда в клетках ДНК и белки притягиваются друг к другу, потому что фосфатные группы ДНК несут отрицательный заряд, а многие аминокислоты — положительный [29].
При этом есть основания полагать, что, по аналогии с физиологией растений, избыток фосфатов будет стимулировать клеточную энергетику (митохондрии), а избыток азотистых веществ (и аминокислот) будет активировать репликационные процессы клеток (рост ткани).
Концепция автора о регулировке экспрессии-репрессии генов через взаимодействие с ними зарядов на их паттернах
Ювентальный реверс – это что? Ювентальные, изначальные эпигенетические паттерны обусловлены изначальной экспрессией ювенильных генов, так как являются отражением их экспрессивности. Первичная полная экспрессия ювентальности начинается на этапе бластулы зародыша, когда происходит сброс всех предшествующих эпигеномных надстроек. Для этого процесса должна существовать некая программа по сбросу, типа очистки флешки. При этом идёт не просто сброс, а глубокая перестройка всех структур и белков, так как они все интегрированы с эпигеномом.
В норме экспрессивные или репрессивные гены всегда поддерживают над собой свой тот или иной зарядо-паттерн. Данный паттерн связан с особенностями зарядов на его генах и комплексом уравновешивающих зарядов как в окружающих паттернах, так и окружающем протеоме, мембранах и ... Такую систему паттернов и открытых-закрытых генов можно представить, как ёлочную гирлянду, где одни лампочки зажжены, а другие потушены. Такое зажигание лампочек соответствует соответствию заряда паттерна и работающему гену. Закрытие паттерна ювенильности ведёт к утрате её и переходу к сенесцентности, то есть работе на новых генах. ДНК – это цепь электростатических зарядов, где «включено»-«выключено» определяет наличие той или иной величины сопротивления на паттерне. Высокое сопротивление ведёт к отключению его. Паттерн может не расстёгиваться и инфо не транскрибироваться даже если это целесообразно для клетки.
Особенности зарядо-паттернов у сенесцентных и онкологических клеток. При этом, автор считает, что сенесцентные и онкологические клетки имеют общие механизмы авторегулировок репликаций и энергетики, и что это две крайности одного и того же маятникового механизма, в условиях, когда клетки в обоих случаях входят в гликолиз, но на разную глубину [25]. В обоих случаях вырабатывается лактат и общий SASP*. То есть, это генетическая развилка, когда в зависимости от преимущества тех или иных генов, процесс может пойти дальше то в одну, то в другую сторону:
- в случае онкологии процесс идёт в сторону сбоя (ослабления) контрпозитных генов регулировок (разрегулировок) и усиления транспозитных (стимулирующих репликации) генов единого механизма авторегулировок, что ведёт к неуправляемой репликации
- в случае сенесцента процесс идёт в сторону сбоя (ослабления) транспозитных генов регулировок (разрегулировок) и усиления контрпозитных генов (тормозящих) единого маятникового механизма.
Разрегулировки являются следствием эпигенеза.
Но начальные стадии развития у сенесцента и возрастной онкологии общие (в том числе и механизмы метавоспаления).
Эту же концепцию подтверждают и данные о положительной противоонкологической направленности действия фосфатов на онкоклетки. Очевидно эти же фосфаты окажут и противосенесцентное действие.
Причём некоторые формы фосфатов (например, маннозо-6-фосфат) накапливается и подавляет глюкозофосфатизомеразу (GPI) и другие ферменты, связанные с метаболизмом глюкозы. Это ухудшает дальнейший метаболизм глюкозы в гликолизе, цикле трикарбоновых кислот, пентозофосфатном пути и синтезе гликанов, что может снижать уровни белков Mcl-1 и Bcl-XL и усиливать апоптоз онкоклеток. Также действие маннозы сказывается на снижении концентрации дезоксирибонуклеозидтрифосфатов (dNTP), из которых и синтезируется ДНК. Манноза глушит гликолизный метаболизм, что и является причиной ухода гликолизных клеток на апоптоз.
С другой стороны, известны данные о пирофосфате магния. Магний главный элемент в стимулировании энергетики в митохондриях для кислородного пути образования АТФ. Фосфаты тоже имеют многочисленные функции, одна из которых ощелачивать и вносить минусовой заряд вокруг ДНК и тем самым влиять на эпигеном, содействуя его ювентальности. Но для этого должны существовать некие механизмы (гомеостаз) автоподдерживания высокого уровня фосфатов. Очевидно, проблема может проявиться не столько из-за дефицита фосфатов, сколько из-за неусваиваемости их, резистентности к ним. На пути стоит некий барьер (-ы), очевидно энергетический и смещённый эпигеном. Это аналогично феномену Варбурга, то есть «негипоксичной гипоксии», или «ложной гипоксии», когда кислорода в среде для клетки достаточно, но она им не может воспользоваться и находится в непрерывном гликолизе и провоспалении. В случае с фосфатами можно говорить о «ложной фосфатной недостаточности». Поэтому могут возникнуть сомнения, что дополнительная подача в организм фосфатов не означает, что они все попадут по адресу, так как гомеостаз у сенесцентных клеток на поддержание уровня фосфатов иной, то есть иные запросы, восприимчивость, возможности утилизации.
У онкологии и сенесцента общей проблемой стоит наличие множества резистентностей, «ложных недостаточностей», это их общая черта. Но каждая резистентность, например, к поступающим ингредиентам, это по сути проявление недостаточной работы конкретного гена контролирующего эту функцию. Но при сенесценте наблюдается множество «ложных недостаточностей», что указывает на эпигеномную их общность. Но главными из этих «недостаточностей» являются кислородная и фосфатная. Очевидно, с восстановлением в них восстановятся и все остальные сбои с «недостаточностями». Явно эти недостаточности связаны с ослаблением в энергетике и фиксированием нового гомеостаза на эпигеноме, а точнее энтропостаза* неполноценности.
Что такое полный или неполный ювентальный реверс?
Именно эти механизмы поддерживания ювентальности представляют для нас основную цель. Во взрослом организме полный ювентальный реверс невозможен, так как это преимущество возможно только при гаметообразовании, когда запускается механизм рекомбинации хроматина. Но говорить о неполном ювентальном реверсе реально и в пределах сформировавшегося организма. Именно здесь автор видит один из выходов на путь ювентального реверса*, то есть вывод из сенесцентного в ювентальное состояние. Но всё же, очевидно, это не тот! механизм полного сбрасывания (очистки) сенесцентных паттернов, который происходит в бластуле. Очевидно механизм такой полной очистки реализуется в период гаметообразования при мейозе, когда происходит редукция с уменьшением вдвое числа хромосом и рекомбинация наследственной информации путём кроссинговера*. Рекомбинация и является механизмом полного сброса сенесцентных паттернов!
При этом при мейозе происходит дополнительное деление и образуется 4 клетки. При таком дополнительном делении очевидно происходит полный сброс всех паттернов и включение только первичного ювентального.
Аналогичные данные по снятию эпигеномных паттернов можно наблюдать в опытах по пересадке ядра опухолевой клетки лягушки в яйцеклетку, из которой предварительно удалили собственное ядро, и при этом выяснили, что из яйцеклетки вырастает здоровый головастик. Это доказало, что рак — проблема не генетической программы, а её ошибочного использования. И эту ошибку даёт эпигеном?! Аналогичная эпигеномная ошибка и при сенесценте? Но эпигеном находится тоже в ядре на хроматине. Но это означает, что истинная первопричинная суть не в эпигеноме, а значит он тоже зависим и, очевидно, от силы энергетики и свойств протеома* в цитоплазме. В приведённом опыте «больному» сбоенному ядру представили свежую цитоплазму яйцеклетки и ядро заработало как нормальное. Но с другой стороны, искаженный эпигеном (энтропостаз) всё же даёт ошибку транскрипции генома и это ведёт к накоплению неверных конформационных и нерабочих белков. В свежей цитоплазме яйцеклетки этот протеом здоровый и под него перестроились эпигеном и митохондрии. Тогда вопрос, что кого предопределяет: эпигеном определяет протеом цитоплазмы или протеом определяет эпигеном? Очевидно, феномен ремодификации раковых клеток можно объяснить степенью доминирования UASP* (противоположность SASP) и протеома у цитоплазмы яйцеклеток. Тогда следует, что пересадка этого же ядра раковой клетки в сенесцентную клетку не приведёт к указанному явлению и клетка останется раковой. Это можно объяснить тем, что сенесцентные клетки имеют схожий гликолизно-провоспалительный SASP и это не позволит перестроить паттерны эпигенома.
Такой неожиданный вывод означает, что с раковыми и сенесцентными клетками можно бороться путём смены их сенесцентного метаболома-протеома и SASP на ювентальный UASP, то есть через механизмы:
- аутофагии,
- парабиогенеза,
- полуавтономии.
Аутофагия нужна для поддержки здорового секретома клетки.
Полуавтономия – под этим термином автор понимает переход на ограниченное питание за счёт оживленных в инкубаторе (5-15 дней) 2-х желтков яиц в день. Конечно это делается не постоянно, а циклами по 3 дня в неделю 4 раза в месяц. Кроме того, для усиления эффекта в конце каждых 3 месяца проводится такое питание в течение 5-7 дней, а в конце каждых 6 месяцев проводится такое питание в течение 14 дней, а один раз в год проводится такое питание в течение 21 дня.
При этом следует учитывать, что при обычном питании кишечник содержит до 5 кг микробиома и это огромная фабрика по ферментированию и сбраживанию пищевых субстратов, а при полуавтономном питании микробиом уменьшится в разы, вплоть до 100 г, а организм будет перестраиваться на экономный режим метаболизма в виде полуавтономии, самовосстановления за счёт внутренних резервов. Для сохранения такой огромной армады микробиома организм вынужден задействовать огромную армию иммунных клеток лимфоцитов, поддерживая лимфоцитоз, что перенапрягает иммунитет. Дополнительно для активирования митохондрий в этом случае автор считает целесообразным применять Mg-цитрат по 1 чайной ложки с тёплой водой 0,5 стакана.
Парабиогенез - в его качестве работает метод ежедневного приёма 2-х оживлённых желтков яиц.
Яичные желтки – это природный источник фосфолипидов (лецитина, холина), что особенно ценно согласно нашей концепции о необходимости усиливать фосфатами минусовой заряд в области ядра и хроматина для поддержания ювентального эпигенома и вытеснения дефектных белков из цитоплазмы.
Прогерийный (преждевременный из-за генетических поломок) путь сенесцента как подсказка сути его механизмов
Этой же позиции соответствуют и данные о прогерийных механизмах сенесцента. В разделе: Разблокировка системы самоочистки клеток обращает сенесцент вспять - показано, что стимулирование работы лизосом — «мусороперерабатывающих заводов» внутри клеток — может помочь в борьбе как с преждевременным (прогерия), так и с естественным старением. В 90% случаев причиной является дефектный белок прогерин, который нарушает нормальную работу клеток, повреждает ДНК, укорачивает теломеры и останавливает процесс деления клеток. Небольшие количества прогерина, да и других дефектных белков можно найти и в организме здорового человека при его обычном старении, а также у пациентов с хроническими заболеваниями почек. Из этого можно сделать вывод, что методы борьбы с прогерином (через аутофагию?) могут помочь не только детям с прогерией, но и обычным людям в борьбе со старением.
Этот вредный белок (очевидно и другие дефектные белки) сначала появляется возле оболочки ядра (очевидно выделяются именно сюда из-за эпигеномно-митохондриальных проблем?), а затем перемещаются в цитоплазму клетки, где он должен разрушаться системой аутофагии в лизосомах — главным механизмом переработки клеточных отходов. Ключевую роль в накоплении внутри клетки вредоносных белков играют лизосомы. У больных прогерией детей эта система очистки плохо работает из-за генетических нарушений. Анализ РНК клеток показал значительное снижение активности генов, связанных с функцией лизосом. В результате прогерин накапливается в клетках, вызывая их преждевременный сенесцент.
Прогерия имеет ряд общих черт с нейродегенеративной болезнью Альцгеймера, где тоже накапливаются дефектные токсичные амилоидные белки повреждающие нейроны. А ведь это одно из обычных проявлений сенесцента, но в конкретной мозговой ткани. Естественно ожидать, что методы аутофагии окажут и здесь положительное действие.
Прогерийный дефектный белок скапливается возле оболочки ядра, а затем перемещается в цитоплазму клетки, где он должен разрушаться системой аутофагии в лизосомах — главным механизмом переработки клеточных отходов. При обычном сенесценте тоже накапливаются дефектные белки, например, с конформационными нарушениями, или липофусцин, или амилоидные белки при Альцгеймере, или... Одной из причин накопления вредных белков является дисфункция лизосом, которая может быть следствием как мутаций, так и нарушения взаимоотношений митохондрий-эпигенома или других причин. Все эти нарушения можно обозначить как «болезни» клеточного уровня. Таким образом на клеточном уровне также, как и на уровне всего организма есть свои как болезни, так и возраст-зависимые «заболевания» (анизомалии*). На уровне клеток тоже есть свои «анизомалии» - анизомодусы* = сенесцентные модусы – инварианты сенесцента. Если разные анизомалии проявляются на уровне систем-органов организма, то анизомодусы – во всём разнообразии морфотипов клеток. Анизомалии – проявления сенилита, анизомодусы – проявления сенесцента. Таким образом, осуществляется сквозная реализация геронтоса на всех уровнях, на всех системах, тканях и клетках. При этом каждый из уровней (этажей) будет преградой для противоположного уровня, противодействовать реювентализации* или реювенилизации*. Это означает, что возврат к ювентосу* (противоположность геронтосу) возможен только при одновременном воздействии в обоих направлениях. Любой сдвиг на любом этаже будет вести к усилению геронтоса и ослаблению Витаукт*. Ни один из этажей ювентоса не может долго сам себя поддерживать при одностороннем возврате к статусу ювенильности или ювентальности на одном из этажей, так как это приведёт к состоянию его неустойчивости. Устойчивость возможна, когда верха и низы – это единая система. Без этого клетки переходят на путь прогерии – ускоренного сенесцента. Каждый из этажей поддерживает статус противоположного. Этим, очевидно, можно объяснить эффект лимита Хейфлика – утраты ювентальности клетками проявляется в изолировании, то есть в культуре ткани.
У больных прогерией детей клеточная система очистки плохо работает из-за генетических нарушений обеспечения этого процесса. Анализ РНК клеток показал значительное снижение активности генов, связанных с функцией лизосом. В результате прогерин накапливается в клетках, вызывая их преждевременный сенесцент. Ключевым словом здесь является преждевременный сенесцент, что может дать объяснение (раскодировать смысл, суть) вообще значения сенесцента в сенилите. Сенесцент это один из инструментов становления, воплощения онтогенеза, механизм ступенчатой его реализации через путь инволюций в тимусе, эпифизе, гипоталамусе…, а затем интервенционное тотальное овладение всем организмом. В случае с прогерией сенесцент идёт не по полноценному сценарию, графику онтогенеза. В данном случае это усечённый онтогенез. Взаиморегулировка, соподчинение сенесцента и сенилита друг другу здесь нарушена. То есть одна сторона процесса здесь не сопряжена полноценно с другой стороной (этажом). Степень сопряжения становления механизмов, реализующих сенилит и сенесцент (на верхних и нижних этажах) ведущих к геронтосу определяет разнообразие типов онтогенеза и динамику прохождения им через ряд ступеней (этапов). Всё это определяет характеристику Онтодианной Линии Жизни.
Эволюция широко использует механизмы усечённого онтогенеза или пролонгированного онтогенеза в видовом разнообразии нужного для оптимизации Онтодианной Линии Жизни путём естественного отбора. Ключевым словом здесь является пролонгированный онтогенез, то есть тот который имеет более широкое окно возможностей. Мыши живут 2 года, землекопы – 27 лет. Становление сенесцента – расписанный по деталям, пошагово процесс. Как вывод, можно утверждать, что сенесцент (в норме развития) это ведомый направляемый последовательно реализуемый процесс. Вначале он зарождается кейлонным путём на уровне клеток в тимусе, что стартирует переход на уровень «штабов» регулировок в верхних этажах и оттуда «спускается» на ткани, а затем на клетки. Сенесцент обуславливает степень реализации сенилита, а сенилит в свою очередь по механизмам обратной связи управляет механизмами разворачивания сенесцента. В определённых случаях ускоренный сенилит может привести к ускоренному растеканию сенесцента (подобно преждевременному сенесценту при прогерии).
Паттерны сенесцента на хроматине ядра оказывают влияние на перестройки в митохондриях, а те в свою очередь перераспределяют взаимоотношения лизосом с дефектными белками и цитоплазмой. При обычном сенесценте избыточные дефектные белки появляются в связи с эпигенезом и его паттерновыми блоками на геноме ядра? Через блоки в ядре происходит вторично и перестройки в системе обновления и функционирования митохондрий, что и ведёт их в сторону гликолиза. Это по системе обратной связи влияет не только на увеличение наличия дефектных белков, с которыми не справляются лизосомы, но и смены метаболома из-за того, что в этот замкнутый круг вписываются и митохондрии? Перекос в эту сторону может усиливать степень сенилитных перестроек (гормонального и иммунного профиля) и инволюций в «штабах» регулировок. Гормоны в процессе созревания организма усиливают процесс сенесцента.
Сенилит* ведёт к перекосам в балансах системы очисток в клетках. В норме баланс выработки дефектных белков из-за эпигеномно-митохондриальных причин всегда нивелируется исправной работой лизосом. Но этот баланс нарушается созреванием организма (адальтус) и его перезреванием (матура). Так статус «верхов» (сенилит) передвигает, определяет перекосы в балансах гомеостазов клеток взаимодействия систем эпигенома-митохондрий-лизосом в сторону их сенесцента. Это, очевидно, и является объяснением причины почему первичные ключи от сенесцента находятся в цитоплазме, а не на эпигеноме и митохондриях.
При этом процессы сенесцента усиливают процессы сенилита, а те в свою очередь тоже усиливают процесс сенесцента. Таким образом, процесс развивается по спирали, раскручивая этапы онтогенеза на Онтодианной Линии Жизни*. Под раскруткой этапов онтогенеза подразумевается реципрокные шаги смещений в балансире регулирующих рычагов между сенесцентом и сенилитом.
Сенесцент сопряжен с нарушением работы лизосом. Такой вывод можно сделать из изложенного. Тогда это означает что преодолевать сенесцент без разработки методов полной аутофагии невозможно.
Каждое из возрастных состояний клеток (фенотипов) имеет свой статус паттернов, свою зафиксированную эпи- надпрограмму, гистоновый код, которая поддерживает свой анизомалийный* гомеостаз = анизомодус* (ущербный или вредоносный). Если ювентальные паттерны – это норма, то сенесцентные и онкологические паттерны - делают клетку плохо управляемой, резистентной, мешают автоматической реализации её генетических возможностей и потребностей. Ремодификация таких клеток невозможна без возврата к норма-паттернам (ювентальным). Но в свою очередь вновь образовавшиеся энергетические или иные анизо-паттерны* (патологически изменённые) не могут поддаваться корректировке, так как они зафиксировали (не пускают) к восстановлению энергетику митохондрий и сами зависят от них: замкнутый порочный круг, когда одно не пропускает другое, процесс необратимый. Верха (эпигеном) не могут управлять низами (митохондриями), а низы не могут откорректировать верха (реализовать свои потенции), так как система стабилизировалась на новых балансах. Каждый гомеостаз – это механизм сохранения определённых параметров относительно нормо-констант = нормо-коридоров, где каждая из них фиксируется определенными генами, а выход из зоны ответственности гена (-ов) (norma-constant) ведёт к выходу за пределы данного гомеостаза. Гомеостаз у таких клеток вышел за пределы нормо-констант (автоматическая система коррекции вокруг оси, относительно которой идёт стабилизация параметра) и за пределами нормо-коридора устанавливаются новые порочные гомеостазы (анизостазы):
- энергоанизостаз* (на основе гликолиза),
- метаболомоанизостаз* (представлены иные функциональные белки).
Это меняет возможности механизмов авторегулировки. Сбиваются механизмы авторегулировки, которые теперь настроены на анизо-константы. Фиксирование нового анизо-паттерна* происходит первично на эпигеномном уровне, что вторично отражается на генном уровне путём изменения транскрипции. Таким образом, можно допустить что нормо-константы регулируются на генном уровне, а нормо- и анизо-паттерны – на эпигеномном уровне.
Некоторые сравнивают ДНК с новеньким цифровым диском, а эпигеном – с лазерной считывающей головкой. По ряду причин эта «головка» сбита так как читаются не те паттерны.
Может ли эпигеном работать в двух ипостасях? Мы описали и предложили возможную роль эпигенома в виде балансира, который способен создавать свои паттерны, фенотипы, модификаты... Но также известно, что гистоны рубашки предназначены для предотвращения неправильного скручивания ДНК и образуют нуклеосомы (из 8 гистонов) для наматывания вокруг них ДНК для образования хроматина. Тогда следует дать ответ почему это не мешает транскрипции и не является ли это чтением «сквозь стены»? Ведь для этого транскрипционная РНК-полимераза (фермент, расплетающий нуклеосому и отводящий гистоны) должна проникнуть сквозь нуклеосому. Такой механизм транскрипции описан, но он не объясняет информационную подоплёку эпигенома.
При этом следует отметить, что если генетическая информация считывается на молекулярном уровне (РНК-полимераза), то эпигеном больше регулируется на уровне конформационном, за счёт электрозарядов, магнитных полей (виртуальная регулировка). Тогда здесь возможен особый «третий этаж» нематериальной регулировки? Известно, что хроматин несёт на себе огромный электростатический заряд в целом, а это значит, что на уровне генов имеются свои заряды, совокупность которых определяет свою конформацию белков, определяющих процесс. Это уже магнитно-электростатический уровень хранения и пользования информацией, нечто похожее тому, как мы записываем информацию на флешку и другие носители информации компьютера. Тогда активность эпигенома регулируется как конформационно (наличием или отсутствием конформированных белков, бракованных, недозрелых, недоделанных), так и статическими зарядами фосфатов? Причем степень насыщенности минусовыми зарядами может определять статус конформации, но минусовые заряды могут быть не обязательно от фосфатов, но и многих других антиоксидантоподобных молекул. Возможно насыщенность конформациями (избыточных или нефункциональных белков) являются проявлением второй ипостаси эпигенома? Очевидно конформационная информация (дезинформация) может играть не меньшую, если не большую, роль в регулировках (разрегулировках) и взаимодействии эпигенома и генома.
Но не означает ли это, что на систему геном-эпигеном можно воздействовать и через информационные поля…? Это более высокие уровни надхроматиновой регулировки…
Белки Теплового Шока (БТШ), очевидно, прямые участники этих конформационных эпигеном-геномных регулировок.
Двухэтажный механизм регулировок клеток
Таким образом, регулировка гомеостазов регулируется на двух разных этажах. Клетка, по сути, это автономное государство. И принципы сдвигов и закрепления в её регулировке (гомеорез*) статусов те же, что и у организма (гормезисорез*), где геронтос = сенесцент + сенилит. На уровне клеток это анизостаз = анизоконстанты + анизопаттерны. Любой сенесцент или онкоперерождение являются анизостазом. Антиподом геронтоса на уровне клеток является ювентос, где ювентос = ювентал + ювентил. Здесь ювентал является заданной программой изначально на уровне клеток, а ювентил - это программа, наведённая эпигеномно, то есть надстройкой. Между ними происходит взаимодействие, обратная связь, стремящаяся приводить систему в исходное состояние относительно constant каждого конкретного генного гомеостаза. Генный гомеостаз определяет эпигеномный гомеостаз и наоборот. Регулировка этих констант опосредована через транс- и контрпозитные механизмы регулировки энергетики и протеомный баланс (белков).
Через эпигеномный гомеостаз идёт коррекция генных программ развития в онтогенезе. При смещении генных программ (их репрессии или экспрессии), то есть переходе на новые программы, они задают условия для коррекции эпигеномной мантии и особенностей регулировок с её стороны. Через эпигеном и сигналы коррекции с уровня всего организма на уровень клеток создаются новые модификаты клеток. Так, например, сенилит создаёт условия для сенесцента. Поэтому корректировать сенесцент возможно только опосредованно через воздействие на эпигеном. В свою очередь все внешние корректировки со стороны становления организма осуществляются через клетки иммунной системы, а не напрямую, как это происходит у растений.
В свою очередь если ювентил поддерживает ювентал, то клетка полностью находится в статусе ювентоса*, но если эпи-ювентил* смещается, то это сказывается на гено-ювентале*; рано или поздно происходит коррекция баланса и система выходит из статуса, основанного на балансе ювентоса. Этот сдвиг ведёт к новым статусам и продвигает в сторону различных модификаций сенесцента. Все промежуточные переходы от ювентоса к сенесценту являются элементами реализации зрелости ткани, появлению новых фенотипов на уровне клеток и онтофизиса* на уровне тканей. Всё это отражается на Онтодианной Линии Жизни. Кстати элементы зрелости ткани используются в механизмах регулировок онтогенеза через многочисленные модификации переходных клеток от ювентала к сенесценту. Здесь тоже статусы и фенотипы определяет принцип доминантности той или иной степени ювентала, ювентила, сенесцента в каждом конкретном типе ткани.
Норма-паттерны и анизо-паттерны - это надстройки на ДНК ядра. В ДНК митохондрий (митДНК) нет гистоновых белков, но здесь имеются свои митохондриальные белки импорта, которые несут свой ряд функций и, возможно, контрпозитное крыло регулировок, то есть тоже могут определять митохондриальные анизо-паттерны.
Что первично: энергетика или эпигенез? Эпигенез (смена гистоновой мантии на ДНК) зарождается на функциональном этапе нарушений энергетики и синтеза белков, а при длительном затягивании процесса, его хронизации ведёт к метавоспалениям* и созданию условий для закрепления статуса дисфункции митохондрии и делает её невозвратной. Это является проявлением неуправляемости и резистентности клеток. В случае если причинные факторы изменений функции клетки могут уйти, то перерождение остаться. Внешне это проявляется в виде появления нового фенотипа, модификации клетки, в том числе сенесцентного, ракового или иного фенотипа.
Митохондриальная недостаточность – основа для функциональной недостаточности клеток. Если митохондриальная недостаточность ведёт к нарушению энергетики клеток, затем к функциональной недостаточности, а значит к недовыработке функциональных белков специализации клеток. Каждый тип ткани имеет свои дифференцированные клетки. Если в организме 16 типов тканей и в нём тотальный сенесцент, то это означает что в каждом типе ткани будут происходить свои функциональные недостаточности = пении, точнее анизопении. Таковыми являются:
- меланопения (недостаток выработки меланина в волосах – причины седины волос),
- саркопения (мышечное одряхление из-за недостатка миозина),
- эпителийпения (одряхление кожи и недовыработка коллагена),
- эндотелийпения (недостаток выработки гликокаликса эндотелия),
- пинеалопения (недостаток выработки мелатонина пинеальной железой),
- нейро- и глиопения (ухудшение работы мозга),
- …
Любая анизопения лежит в основе анизомалий*, а анизомалии лежат в основе сенилита и феноптоза (механизм возрастной самоликвидации организма).
Весь комплекс пений является основой для сенилита. Таким образом митохондриальная энергонедостаточность (энергоанизостаз) является основой для сенесцента (клеточного старения), а функциональная недостаточность (метаболомоанизостаз) – основа сенилитных перерождений всех тканей и сенилита в целом. И, как видим, одно исходит из другого (сенилит из сенесцента). Все анизопении зиждутся на сенесцентных анизо-паттернах и анизо-константах.
Откуда идут корни, начала митохондриальной недостаточности? Исключим варианты ответов, что это износ, клеточный стресс, лимит Хейфлика и другие механические «причины». Нет, так как эти статусы не случайны для клетки, а коммитированы* ей как обязательное проявление на определённом этапе. Этот эпигенез обязателен к исполнению, это рычаг к регулировкам и к появлению новых фенотипов. Таким образом, эти же механизмы эпигенеза важны для реализации продвижения по Онтодианной Линии Жизни (ОЛЖ).
Что такое «окно возможностей»? Вся эта Онтодианная Линия коммитирована. Все высшие потенции как плюрипотентность и др. заблокированы после эмбрионального этапа, что исключает регенерацию и полную репарацию, а также предусматривает смещение баланса с ювентальности на сенесцент. Коммитации строго участвуют в системе регулировок всех этапов онтогенеза и реализуются через балансы ЮК/СК посредством эпигенеза. Таким образом, после эмбрионального периода возможности организма строго ограничены некими «окнами возможностей», которые также называют запасом возможностей или критическим окном, за пределами которого исключаются механизмы продления существования особи. Причём у каждого вида это Окно Возможностей имеет свои пределы, оно реализуется в определённых рамках продолжительности времени существования, которая на ОЛЖ и обусловлена спектром коммитаций. Этот же рычаг руководит соотношением или доминантностью ювентальных (ЮК) и сенесцентных клеток (СК). Особенно это важно на начальных этапах для появления зрелых гиперфункциональных тканей. То есть через баланс ЮК/СК идёт становление новых фенотипов тканей. Вначале наступает зрелость, компенсаторное повышение функциональности ткани, но при наращивании дисбаланса – гиперфункция и дегенерация. На определённых этапах этот баланс ЮК/СК доходит до критического сенесцентного доминирования, когда возможности такой системы полностью исчерпаны. Выход здесь только один – сохранение ювентальной доминантности.
Что ведёт к митохондриальной недостаточности или их подавлению? В первую очередь это могут быть:
- сигналы от других тканей в виде SASP,
- белок ReHMGB1, который «заражает» сенесцентом и «гасит» ювентальность,
- продукты «неполного сгорания»,
- гликолизные метаболиты,
- воспалительные интерлейкины,
- затем (вторично) усиливается роль смены гормонального фона,
- ...
Следует понимать, что баланс ЮК/СК определяет элевацию и инволюцию в гормональных «штабах» регулировок (тимус, эпифиз, гипоталамус…). Эти штабы зависят от иммунного статуса в них. То есть статус сенесцента на клетки наводится. В ювенальном возрасте практически все клетки ювентальны, в возрасте 35 лет баланс ЮК/СК уравновешен, а в возрасте 65 лет этот баланс в 10 раз перевешивает в сторону СК.
В чём особенности митохондрий в сенесцентных клетках? Напомню, что сенесцентные клетки теряют способность к репликациям и частично к репарациям, а это означает что энергетически их митохондрии продолжают работать, но пластические процессы, отвечающие за дифференцировку и высшие функции клетки, в т. ч. и выработку белков специализации, эти клетки не производят в достаточном количестве. Многие высшие клетки при этом часто теряют свою специализацию, например, адипоциты превращаются в примитивные виброциты, также этот процесс наблюдается и во многих других типах тканей – снижение ранга дифференцировки. Но за дифференцировку должны отвечать программы в ядре клетки. Тем не менее, появились работы, которые указывают на исходную точку этих процессов из митохондрий и подтверждающие митохондриальную природу эпигенеза сенесцента.
Проанализируем статью: «Ученые обнаружили «разделение труда» в митохондриях» [30]. В ней приведены данные научного исследования показывающие, что митохондрии отвечают не только за энергетику клетки, но и за производство ряда специфических белков. Но энергетика и репарационный синтез это два самостоятельных процесса, конкурирующие между собой. Оказывается, в митохондриях решена эта проблема путём специализации митохондрий на два типа:
- одни из них сосредоточены на производстве энергии в виде АТФ,
- а другие - на синтез некоторых аминокислот, входящих в состав белков, и других необходимых молекул.
Да, конечно, часть аминокислот мы получаем с пищей, но этого внешнего сырья митохондриям недостаточно для выполнения своих высших специализированных функций и ферментов. Чтобы синтезировать аминокислоты и особые белки, органеллы должны перенаправить молекулы, которые в противном случае пошли бы на производство АТФ, что потенциально снижает производство энергии в клетке.
Исследователи выращивали мышиные клетки на культуральных смесях, которые заставляли клетки получать энергию исключительно из митохондрий, а не из альтернативных реакций, генерирующих АТФ. Хотя клетки увеличивали производство энергии митохондриями, органеллам все равно удавалось синтезировать аминокислоты. Казалось бы, «один процесс должен был красть ресурсы другого». Но обнаружили, что в клетках мышей, лишенных питательных веществ, молекулы P5CS скапливаются только в некоторых митохондриях. P5CS ключевой митохондриальный фермент, который собирается в нити, помогающие органеллам катализировать один из этапов образования аминокислот. Обнаружили, что в клетках мышей, лишенных питательных веществ, молекулы P5CS скапливаются только в некоторых митохондриях.
Митохондрии, в которых находились кластеры P5CS, имели еще два отличия. Во-первых, в них отсутствовал фермент, который производит АТФ. Кроме того, у них отсутствовала складчатая внутренняя мембрана, которая повышает эффективность производства АТФ.
Стало очевидным, что в клетках, испытывающих дефицит питательных веществ, образуются два подтипа митохондрий, которые сосредоточены на:
- либо выработке энергии,
- либо строительстве молекул.
Эта способность митохондрий к дифференциации на энергетические и пластические функции зависит от их способности сливаться во едино или разъединяться, тем самым способствуя тому или иному процессу. При этом создаются разные фенотипы митохондрий, выполняющих разные функции. В норме специализация митохондрий похоже идёт в пределах одних и тех же клеток и митохондриях, при нагрузках или проблемах процесс разъединяется по разным митохондриям. Похоже, в зависимости от того в какой степени происходит это разъединение, процесс будет отражаться и на проявлении клеточных модификаций и фенотипов.
В свою очередь такой перекос в функциях митохондрий в сторону энергетики или синтеза базовых белков зависит не только от внешних факторов, но и от эпигенетических коррекций и переводить процесс из функционального в структурный статус, «консервируя» его.
Этому же помогают и митохондриальные рибосомы (отвечают за синтез белков в митохондриях, обеспечивающих аэробный путь), которые имеют свои ДНК, и их активность может быть перестроена под внешние эпигенетические перестройки. В свою очередь рибосомы в цитоплазме клеток тоже участники сенесцента. Это подтверждают данные о том, что участок ДНК ядерного хроматина, который ответственен за рибосомы, подвержен особо высокому уровню метилирования, как показатель сенесцента. До момента полового созревания в организме человека активно поддерживается работа рибосомной ДНК — участка генома, необходимого для выживания клеток. В зрелости его эффективность снижается, что запускает молекулярные механизмы старения. Ученые оценивали два показателя: число копий рДНК и уровень их метилирования — химической метки, которая «отключает» активность гена. У детей и подростков число активных (неметилированных) копий не уменьшается, а наоборот — несколько возрастает. Это означает, что клетки в юном возрасте поддерживают работу рДНК в «молодом» состоянии. У взрослых же наблюдается противоположный процесс: с возрастом активных копий становится меньше, а уровень метилирования — выше. Значит глушится работа «цеха» по воспроизводству белков важных в работе ювентальных клеток. Почему «глушится» - очевидно это связано с дефицитом кислородной энергетики митохондрий.
Итак, двоякие свойства митохондрий позволяют пересмотреть проблему понимания отличия ювентальных клеток от сенесцентных и раковых, которые имеют ограниченные возможности пользоваться кислородной энергетикой и переходят в гликолиз, что объясняет снижение производства базовых белков специализации. Эта ограниченность даёт преимущества сенесцентным клеткам и позволяет им глушить ювентальные (стволовые). Ограничивается потенциал репараций – самовосстановления. Возникает проблема сенолитизма – устранения, очистки от сенесцентных клеток.
Здоровые, то есть ювентальные клетки обладают одновременно высоким уровнем не только митохондрий, отвечающих за энергетику, но и митохондрий обеспечивающих выработку белков специализации, которые нужны для высокофункциональных специализированных клеток, то есть повышающих резко производительность, работоспособность клеток, которая зависит от способности клеток развивать особо высокую мощность, основанную на кислородной энергетике.
Узким (слабым) местом у сенесцентных клеток является регулировка митотического цикла, когда клетки останавливают способность к делению на фазе G1, что проявляется в виде ареста митотического цикла. Очевидно арест — это недостаточность, недовыработка индукторов митоза, ограниченные силы для этого. Это означает что при отсутствии и недостатке митохондрий фенотипа MF2 (отвечают за специализированный синтез функциональных белков) сенесцентные клетки прекращают делиться. Но они могут еще долго существовать за счёт митохондрий фенотипа MF1 (создают и используют энергию, но не приносят функциональной пользы). В некоторых отношениях им подобны и раковые клетки: недостаток митохондрий фенотипа МF2 – сопряженных с особой энергетикой, обеспечивающей синтез особых белков для специализации.
У здоровых клеток деятельность MF1 и MF2 сбалансирована и взаиморегулируема. У онкологических и сенесцентных клеток баланс смещён в сторону снижения MF1 (с учётом их уклона на гликолиз). Но в тоже время деятельность митохондрий MF2 тоже недоразвита. Эта модификация митохондрий и является причиной утраты ювентальности и перехода на сенесцент.
Раковые и сенесцентные клетки связаны с базовыми митохондриальными проблемами – это утверждение основано на ряде данных. В обоих случаях недоразвито крыло митохондриальной деятельности с функциями МF2, с застреванием в гликолизе.
Причины особенностей раковых клеток. Они сохраняют способность к делению, митозам! Почему? Похоже не срабатывает другая цепочка генов-регуляторов и не вырабатывается группа контрпозитных белков торможения митоза, а не транспозитные механизмы активации митоза. Тогда значимость белков-контрпозитов выше чем белков-транспозитов? Активность транспозитов контрпозитов автоматически регулируется реципрокным механизмом. Следовательно, онкоклетки запускаются на этапе, когда не запущен еще механизм сенесцентности. Такое возможно, когда происходит перескок этого порога сенесцентности, но сразу запустили контрпозитную недостаточность. Очевидно правильнее понимать, что они не перескочили, а не дошли до блока транспозитных сенесцентно обусловленных генов, контролируемых эпигенезом. В противном случае блок транспозитных генов недовёл бы этот процесс до контрпозитов. Поскольку в обоих случаях сенесцента и рака проблема связана с митохондриальной недостаточностью, то следует искать нарушения в первую очередь не на уровне ДНК ядра, а на уровне ДНК-митохондрий. А вообще регулировка митохондрий и митозов происходит двояко: как на уровне ДНК ядра, так и на уровне ДНК митохондрий. Это один из вариантов проявления MF2 митохондриальной недостаточности, когда энергетика клеток особо усугублена?
Почему у МF2 могут быть такие разные фенотипы клеток? В обоих случаях отмечается митохондриальная дисфункция, при которой происходит падение электропотенциалов на мембранах клетки, включая митохондрии, ЭндоПлазматическийРетикулум, ядра. Очевидно различия связаны с разной величиной падения этих потенциалов: у сенесцентных клеток он снижается с -70 мВ до -50 мВ, а у онкологических – до -40 мВ. Этого достаточно чтобы изменить состояние эпигенома. Различная степень дисфункции!? Различный запуск опосредованных эпигеномно экспрессий, например, в ядре клетки ген р53? Тогда следует говорить о дисфункциональных подтипах среди типов MitFen2, то есть о MitFen2/Dis1 (сенесцентный) и MitFen2/Dis2 (раковый). В обоих случаях и раковые, и сенесцентные клетки связаны с недовыработкой потенциалов, но параметры недовыработки существенно различаются, что и запускает разные эпигеномные паттерны и сдвиги сказываются на работе разных генов? Сенесцент и онкология – два противоположных крыла одной системы репликаций. Клетка как бы упускает из рук вожжи самоуправления и согласовывания их с потребностями целого. Это означает выход за пределы гомеостазов, где невозможно ауторегулировка клетки. Вместо автозапуска механизма возврата к гомеостазу (центропии) запускаются механизмы энтропии, усугубления проблемы, то есть в противоположном направлении и раскачивания клетки в неуправляемые процессы.
Что такое БИОКРИСТАЛЛ или Магический кристалл?
Автор исходит из позиции, что хроматин — это БИОКРИСТАЛЛ, то есть подобен пьезокристаллу, когда любое воздействие на него формирует электрический заряд или под действием электрического напряжения кристалл меняет форму, например скручивается. Пьезоэлектрический эффект – результат поляризации диэлектрика под действием различных причин. При этом происходит смещение связанных зарядов или поворот диэлектрических диполей. Очевидно роль таких диполей играют гистоны в гистоновой рубашке. Гистоны – ядерные белки, которые входят в состав хроматина и содержат положительно заряженные аминокислоты – лизин и аргинин, что позволяет им взаимодействовать с отрицательно заряженными фосфатными группами ДНК и нейтрализовать их заряд. Гистоны обеспечивают компактную упаковку ДНК. Гистоны действуют как катушки (нуклеосомы), вокруг которых наматывается ДНК. Гистоны участвуют в эпигенетической регуляции транскрипции, репликации и репарации. Они же участники и модификаций. Это же может происходить и под действием различных магнитных полей и др. сил. Важной особенностью такого заряженного хроматина является автоподдержание баланса в электростатической намагниченности в каждом из звеньев, образующихся при спиральном скручивании двухцепочной нити ДНК. При этом любое локальное изменение влияет на общее механическое напряжение во всей цепочке и нарушает транскрипцию. Каждая функциональная скрутка (звено) должна лечь в своё ложе (гнездо) и образовать свой функциональный паттерн (гистоновый код).
Эпигенез сенесцента и онкологии ломает механизм нормального скручивания и транскрипции. При этом паттерны ложатся не в своё ложе (гнездо) и начинается путаница в скрутках, образование узлов в хроматине с потерей зарядов на некоторых паттернах, что делает их невидимыми или наоборот. Очевидно каждая скрутка обладает зарядом как на обкладках конденсатора, что поддерживает хромосому как в подвешенном состоянии на плаву в электромагнитном поле. Но в любом случае (сенесцент или онкология) нарушена энергетика и разность потенциалов, причём в разной степени. Сенесцент – следствие гистоновых модификаций. Онкология – тоже является проблемой гистоновых модификаций, а не мутаций.
Автор предлагает концепцию, что ювентальные или сенесцентные клетки имеют каждая свой эпигенетический статус (эпигенотип) и свою эпигенетическую среду – эдафотоп. Каждый эдафотоп - это, по сути, ландшафт-ниша, которую определяют, как свои внутриклеточные SASP или USAP, так и выделения на уровне всего организма, включая продукты ОАС, общий метаболом, гормональный фон и др… В совокупности они могут обусловливать определённый статус преобладания процессов метилирования или ацетилирования на гистоновой рубашке и в определённой системе её паттернов (эпигенотип). Каждый эпигенотип может существовать в условиях своего эдафотопа или другими словами каждый эдафотоп имеет свой эпигенотип.
Искусственная смена эдафотопов скомпенсирует недостающие механизмы нужные для реювентализации
При этом каждый эдафотоп имеет свою настройку генных сенсоров, сопряженных с ним. Эта настройка реагирует на смену градиентов, которая может быть обеспечена как параметрами количественного роста, так и параметрами качественных изменений (рост заменяется на процессы зрелости). В итоге в пределах этого эдафотопа как открытой ламинарной системы создаются условия для смены градиентов, что ведёт к эпигенезу, появлению новых эпигенотипов. Такой процесс в организмах животного типа в этом случае может идти только в одну сторону, так как отсутствуют механизмы для обратного реверса. Но теоретически можно утверждать, что если мы искусственно будем менять среду эдафотопа, то тем самым будем компенсировать отсутствующие механизмы обратного реверса и реювенилизации.
Может возникнуть вопрос, что лимит Хейфлика в культуре ткани сохраняется даже если клетки содержать в ювенильной питательной среде. Ряд данных показывает, что здесь возникает новый эффект изоляции клеток от целого организма, что и является проявлением лимита Хейфлика.
Каждый статус эпигенома или эпигенотип приспособлен к своей нише, что и проявляет сенесцентность или другие модификации клеток
Причём эта эпигенетическая ниша реагирует как на сигналы со стороны УКАС (Универсального Клеточного Адаптационного Стресса), так и со стороны ОАС (Общеорганизменного Адаптационного Стресса по Г. Селье), то есть стресса со стороны на уровне всего организма в виде анизомалий*, хронических заболеваний, стрессов, смены гормонального фона, медиаторного, иммунного, нейрогенного, сенесцентного, сенилитного и др. Таким образом, даже переход на этап адальтуса (возрастной зрелости) или матуры, то есть переход за климактерический рубеж (начала проявленного старения организма), как и множество других факторов, являются триггерами для системного провоспаления, которое неизменно будет только усиливать сенилит. Все они функционируют за пределами коридора Великого Гормезиса, где пожар провоспаления не только тлеет или разгорается, но и затем и бушует. Последствия этого пожара проявляются в виде фиброзирования, склероза ткани, дегенеративных процессов, хронической слабости, истощения Жизненной Силы (клеточного потенциала)…
Старение = геронтос запускается с разных сторон = граней (биокристалла), но в любом случае у них общий неспецифический знаменатель = ОАС + УКАС. Эта сумма является сутью, платформой для сенилитирования. Таким образом, хроматин в целом с его эпигеномной рубашкой – это единое целое, то есть проявляет свойства чувствительного биокристалла-сенсора-дисплея с универсальным характером реактивности на все неспецифические стрессы на любом уровне организма и выдающем в любом случае единый универсальный ответ в виде сенесцента или модификаций иммунных клеток или онкологии.
Концепция автора об организме как о ламинарном Биокристалле. Именно соотношение и объёмы сдвигов в процессах ацетилирования, метилирования и др. в эпигеноме являются определяющим условием неспецифического ответа хроматина на многочисленные и разнообразные сигналы. По сути, это одна из граней реактивности биокристалла хроматина в целом. Это означает что в одном случае (статусе) кристалл выдаёт один ответ на стимул, а в другом случае на тот же стимул даёт другой ответ. Такая разность ответов задаётся свойствами его кристаллической решётки, функцию которой определяет иммунная система и, в частности, её клетки макрофаги-резиденты, которые имеются вокруг всех функциональных клеточных систем.
Возможно, онкология — это непроизвольная митохондриальная аберрация, а сенесцент – произвольная, неизбежная, которая определяется как со стороны онтофизиса (на уровне гормезиса*, то есть возрастных за пределами клеток настроек и ограничений), так и со стороны клеточной коммитации (предопределённость, предписание).
Сумма всех хроматиновых зёрен во всех клетках представляет собой кристаллическую решётку единого Биокристалла в рамках всего организма. Решётка пронизывает весь кристалл и, по сути, представляет собой иммунные клетки-резиденты. От их статуса зависит выбор ответа функциональных клеток в соответствии с предписаниями на Онтодианной линии Жизни. Первые динамические изменения в этом ламинарном (текучем) Биокристалле зарождаются в тимусе и затем сигнал передаётся на эпифиз, приводя его к сенесценту и дегенеративной инволюции (сенилит), что является сигналом для гипоталамуса, а затем процесс разворачивается по принципу домино. Постепенно захватывая все ткани и системы организма. Любые изменения в этой решётке осуществляются через SASP и сенесцент, эта решётка пронизывает организм и даёт универсальную реакцию УКАС, а в последствии и ОАС. Клеточное старение является для организма банальным стрессом.
По сути, такой изменчивый Биокристалл напоминает Магический Кристалл, который может по разному светиться при задавании ему вопросов, то есть обладает чувствительностью и выдаёт соответствующие ответы (реакцию) на задаваемые вопросы. Причём вопросы к Магическому Кристаллу должны быть построены так, чтобы он мог отвечать однозначно на них: «да» или «нет». В биологическом понимании это «специфический» или «неспецифический» ответ. Такое понимание означает, что у этого Биокристалла есть ряд неспецифических рычагов управления, которые могут его сдвигать в ту или иную сторону, в том числе и дать обратный ход – реювентализации.
Как механизмы метилирования и ацетилирования регулируют SASP и кристаллическую решетку с её эпигенезом, обуславливают сенесцент и реакции УКАС?
Всё начинается с ферментативного метилирования цитозина, то есть посадки на него метильных групп, что меняет свойства ДНК.
Количество 5-метилцитозина в ДНК меняется в разные периоды жизни организма:
- от максимального - при рождении,
- до минимального - у дряхлого от старости.
Это указывает на то, что старение регулируется эпигенетически – то есть путём механизма вызывающего длительное и стабильное изменение экспрессии генов. Идёт непрерывная смена эдафотопов и эпигенотипов. Это и есть основа всех возрастных цепочек преобразований на Онтодианной Линии Жизни (ОЛЖ), где сенесцент обуславливает пубертат, адальтус, матуру, сенилит и связанные с ним анизомалии* и мортус (феноптоз*), а сенилит инициирует (разжигает, усиливает) сенесцент. То есть сенесцент ![]() сенилит. Таким образом, ОЛЖ прописана не в геноме, а на эпигеноме. Этим механизмы ОЛЖ отличаются от морфогенеза (генетических программ). Для этих целей выделены эволюционно особые эпигенетические механизмы для реализации ОЛЖ. Регулировка этих эпигенетических механизмов осуществляется через эпигенотипы (градиенты метилирования, ацетилирования и др.) и эдафотопы (градиенты SASP UASP и др.)… Внешне это происходит за счёт смены уровня метавоспалений (первичных), затем провоспалений и связанных с ними апоптозов, снижения силы аутофагии, митохондриальных и иных дисфункций, запуск или отключение генерализованного генного G1/S блока (или разблокировки) для регулировки процессов пролиферации…
сенилит. Таким образом, ОЛЖ прописана не в геноме, а на эпигеноме. Этим механизмы ОЛЖ отличаются от морфогенеза (генетических программ). Для этих целей выделены эволюционно особые эпигенетические механизмы для реализации ОЛЖ. Регулировка этих эпигенетических механизмов осуществляется через эпигенотипы (градиенты метилирования, ацетилирования и др.) и эдафотопы (градиенты SASP UASP и др.)… Внешне это происходит за счёт смены уровня метавоспалений (первичных), затем провоспалений и связанных с ними апоптозов, снижения силы аутофагии, митохондриальных и иных дисфункций, запуск или отключение генерализованного генного G1/S блока (или разблокировки) для регулировки процессов пролиферации…
Выявлено ярко выраженное глобальное уменьшение степени метилирования ДНК во всех органах! нерестящейся горбуши, которая после нереста очень быстро погибает от внезапно наступившей остро выраженной старости. Очевидно такое тотальное снижение метилирования связано с мощным ураганом провоспаления. Аналогичное понижение уровня метилирования ДНК и запрограммированная гибель наблюдалась и у таких растений как бамбук и агава – процессы, которые запускались только после цветения этих растений. Снижение уровня метилирования произошло в связи с ростом гормонального стресса от цветения, которое сопровождается ростом гигантского уровня стресса в виде гормона стресса - абсцизовой кислоты. То есть любой стресс (даже физиологический – цветение) уменьшает метилирование. Это происходит как у растений, так и у животных. Движение по ОЛЖ тоже для организма является стрессом. Острый стресс – является критическим и началом для запуска механизмов мортуса, слабый стресс – запуск компенсационных механизмов. Удалив этот цветоносный побег (у агав, сельдерея и других лимитировано живущих видов…) можно надолго остановить этот процесс старения-стресса-метилирования (лимитирование, предписание сроков жизни на ОЛЖ) и предотвратить резкое понижения уровня метилирования. Попутно отмечу, что в цветоносах и созревающих в них семенах (например сельдерея) вырабатывается огромное количество гормона зрелости и старения и отмирания органов – абсцизовой кислоты (АБК), высокий уровень которой может перевести растения с многолетнего жизненного цикла на 1-летний (арабидопсис) или 2-летний (сельдерей), или 7-15 (агавы) или 100 лет (бамбуки). Очевидно это же происходит и у бамбука – растения монокарпика, которое плодоносит 1 раз в жизни (100 лет) и при этом вырабатывается такой гипервысокий уровень АБК в его соцветиях, который не совместим с жизнью, так как старение затрагивает не какие-то отдельные органы, например плоды или ветки, листья…, а всё растение целиком. Растение само себя уничтожает! Низкий уровень метилирования может привести к отключению механизма пролифераций через торможение генерализованного генного блока G1/S или снижение уровня функциональной активности клеток через митохондриальную дисфункцию, или их гиперфункционированию (работа в разнос с инволюцией в итоге). Всё это различные механизмы наведённых эпигеномно клеточных дисфункций или сенесцента, а на уровне организма - адальтуса и сенилита. Аналогичное очевидно происходит и у агав, которые зацветают один раз в жизни (около 15 лет) и погибают. Удаление цветоноса у агав может продлить жизнь растению до 70-90 лет. Но у родственника агав - столетника древовидного нет такой жесткой элиминации и оно может цвести многие десятки лет жизни, что говорит о том что гормон смерти-старения-стресса АБК здесь не достигает критических уровней. То есть, его то или иное действие определяется через уровень его градиентов. Разные градиенты определяют разные эффекты. При этом у деревьев АБК может приводить к отмиранию (усыханию) неработающих ветвей, осеннему апоптозу в черешках листьев, что ведёт к их локальному опаданию, но не к гибели всего растения. Но если уровни АБК чрезмерны, то апоптоз переходит в феноптоз. При одних уровнях (градиентах) АБК выступает в роли регулятора роста кроны растения или стимулятора созревания, в других – в роли инициатора феноптоза или онтофизисных проявлений. С возрастом в кроне однако уровень АБК всё равно нарастает. Многие растения этому могут противопоставлять ряд механизмов и продолжать существование, но на более высоких уровнях гормонального производства. Такие растения как бы заново восстанавливаются за счёт противодействующих гормонов старению и смерти – ауксины, цитокинины… Это противоположные рычаги регулировок единой маятниковой системы, регулирующей ОЛЖ и противодействующей снижению уровня метилирования (удержанию его нужного баланса). Доминирование гормонов омоложения определяет безлимитные возможности вегетативного пролонгирования существования растения. Доминирование гормона стресса-зрелости-старения-смерти определяет жесткий срок на Онтодианной Линии Жизни: 1- или 2-летников. Быстрое снижение общего уровня метилирования ДНК наблюдалось при старении однолетнего растения Арабидопсис, но не тогда когда оно по разным причинам превращалось в многолетник. Кроме того, была найдена мутация drdl-6, которая воздействуя на механизм регулирующий старение листьев с помощью RdDM (RNA-directed DNA methylation), т. е. через микроРНК воздействующую на метилирование ДНК, вызывала резкое замедление старения листьев Арабидопсиса.
Чемпион по уровню метилирования ДНК Секвойя вечнозелёная (24% генома, тогда как у мыши их всего 4%, а у винной мушки 0,03%). Это говорит о том, что долгоживущие виды имеют более высокие уровни метилирования и что оно сопряжено с генной настройкой на преобладание гормонов омоложения. То есть рычаг омоложения преобладает в этой маятниковой системе. Уровень метилирования эпигенома (ДНК) у человека меняется с возрастом. Это связано с процессом «эпигенетического дрейфа» - смещения, постепенного изменения профиля метилирования ДНК. По одним данным, доля метилирования цитозина в геноме человека в норме составляет 80-90%, по другим – 70-80%. Очевидно это зависит от возраста.
В номе CpG-островки обычно характеризуются низким уровнем метилирования и формируют области открытого хроматина. В то время как CpG-сайты, расположенные за пределами островков, наоборот, чаще всего гиперметилированы.
Высокий уровень метилирования у Секвойи сопряжен с высоким уровнем гормона молодости растений – цитокинина, который вырабатывается в апексах корней. У многих видов растений имеется механизм ювентального реверса, что позволяет им существовать неограниченно долго, реализуя вегетативные механизмы.
У рыбы горбуша при нересте тоже происходит резкое снижение метилирования и смена гормонального фона. Важен ответ на вопрос что здесь первично: эпигеномные сдвиги в метилировании (эпигенотипы – они создают иммунные модификаты) или смена гормонального фона определяет метилирование (эдафотопы)? Известна концепция «эпигенетического дрейфа» - постепенного изменения с возрастом профиля метилирования. В ДНК эмбрионов и новорождённых присутствует наибольшее количество метилированнных цитозиновых оснований (высокое метилирование). Болезни и стрессы оказывают существенное влияние на эти процессы. Например, у мужчин с тяжелым детством уровень метилирования ДНК в области генов, влияющих на развитие мозга плода, был ниже на 19-21%, чем в контрольной группе.
Долгое время считалось, что старость сопряжена со сниженным уровнем среднего метилирования. Однако затем было показано, что во многих тканях такие изменения носят локальный характер и носят разнонаправленный характер.
Важно: процесс возрастного деметилирования может быть ускорен при различных патологических условиях, в частности при различных возраст-зависимых заболеваниях или анизомалиях, таких как рак и болезни иммунной системы.
Метилирование – это по сути процесс глушения генов.
У организмов животных нет гормона стресса – абсцизовой кислоты и старение регулируется совершенно на иных принципах. Старение здесь начинается с клеточного уровня (первичное коммитирование), что ведёт к метавоспалениям и первичному сенесценту в штабах регулировок (эпифиз, тимус, гипоталамус…)… в итоге сенесцент определяет сенилит и из локального уровня интервенционно переходит на тотальный уровень. В итоге сенесцент и сенилит реализуют геронтос.
Механизм сенесцента здесь зарождается в тимусе. Его сигналы передаются на макрофаги-резиденты эпифиза, что ведёт к метавоспалениям в нём, то есть высокого уровня клеточного гормона стресса-зрелости-сенесцента-смерти. Это изменяет функциональную активность эпифиза и ведёт к смене градиентов выработки мелатонина – прототипа цитокининам – гормонам молодости у растений.
Таким образом, у животных драйверами эпигенеза (образование эпигенотипов) являются балансы клеточных гормонов цитокинов провоспалений (прототип абсцизовой кислоты) и общеорганизменного гормона – мелатонина (прототип цитокинина – гормона молодости у растений), а регулировка осуществляется с двух уровней: клеточного и общеорганизменного. Всё зависит от того какой рычаг маятника в итоге перевесит. А это означает, что через этот маятниковый механизм можно влиять на механизмы реювентализации.
Научно подтверждено, что мелатонин может влиять на метилирование ДНК и эпигенетические механизмы в клетках. Мелатонин может влиять на эпигенетические модификации в клетках, например через ремоделирование гистонового белка.
В свою очередь также доказано что провоспалительные цитокины тоже определяют уровень метилирования и сенесцент. Это осуществляется через эпигенетический механизм регуляции экспрессии генов. Это связано с тем, что цитокины стимулируют воспалительный ответ, а метилирование ДНК влияет на активность генов, в том числе цитокинов.
Автором книги «Биология молодости» проведён анализ на эту тему и показано, что особенностью животного мира является то, что всё здесь опосредуется через иммунную систему.
Как происходят энзиматические модификации гистонов при старении? Гистоны это щелочные белки, участвующие в упаковке ДНК в ядре, (ДНК намотана на множество состоящих из гистонов катушек-кассет, называемых нуклеосомами) и одновременно выполняющие функцию структуры регулирующей, под влиянием их эпигенетических модификаций, такие процессы как транскрипция, репликация, репарация.
Ферменты модифицирующие гистоны обычно объединены в комплексы из многих белков… Они образуют гистоновые метки, которые играют важную роль в процессах регулировки продолжительности жизни. Например, ингибирование фермента уменьшающего степень метилирования метки не активного хроматина в ответ на дисфункцию митохондрий, препятствует активации механизма, реагирующего на развёрнутые белки – консервативного механизма препятствующего ускоренному старению.
Обнаружено, что некоторые важные для понимания, изменения метилирования ДНК, происходят главным образом в районах так называемого бивалентного хроматина. Особенностью бивалентного хроматина является то, что на таком хроматине обычно расположен ключевой набор онтогенетически регулируемых генов, которые характеризуются тем, что несут сразу два (би — «дважды») типа меток гистона H3.
Что такое Великий Гормезис?
Состояние Единства Биокристалла (организма) регулируется через синхронность и резонанс всех его гомеостазов во всех системах. Эта синхронность гомеостазов определяет гормезис организма, когда проявляются в максимальной степени интеграция и вся мощь его Витаукта на общеорганизменном уровне и Жизненная Сила на уровне клеток. Такое сквозное взаимовлияние позволяет всем системам ориентироваться в развитии и состоянии относительно друг друга и производить самонастройку и подстройку через эпигенез. Синхронность работы оптимизирует все системы и является ориентиром, компасом для каждой из них. По этому «компасу» все системы и клетки в системах настраиваются на единое целое. Для этого у них имеется система механизмов генетической настройки (клавиатура) или свои «компаса» (чувствительные дисплеи) взаимокорректировок и одновременно регулировок на единое целое. Когда всё работает синхронно и проявляется в высшей степени оптимизированный Витаукт, то в этом случае можно говорить о Великом Гормезисе.
Как видим Великий Гормезис состоит из сочетания единства работы гомеостазов и гормезисов на различных этапах Онтодианной Линии Жизни. Эта Линия определяется через механизмы гормезисореза (механизмы возрастного смещения параметров гормезиса). То есть внешняя часть биокристалла контролирует внутренний клеточный уровень и наоборот. Всё пронизано взаиморегулировками. В такой системе в идеальных биокристаллах возможно вмешиваться через любой уровень регулировок и получать единый общий универсальный ответ на оздоровление или на затухание всего Биокристалла.
Как вернуть организм в зону Великого Гормезиса?
Это возможно только путём возврата клеткам Жизненной Силы. Это не возможно без пролонгирования доминирования ювентальности, значит через подключение ювентального реверса. Запуск этого реверса возможен только при условии возврата прежней эдафической* среды (той или ниши для клеток). Это позволит вернуть в исходный статус эпигенотоп. От него зависят эпигеномные механизмы запуска сенесцента или ювентальности, которые осуществляются через механизм генерализованного G1/S блока (или разблокировки) для процессов пролиферации. Каждый модификат (сенесцентный или ювентальный) может существовать только в своих внешних условиях среды, что обусловлено ориентированностью его генов (эпигенома) только на свои градиенты внешних условий. Таким образом удастся вернуть прежние паттерны и перезапустить изначальные гомеостазы, а затем и гормезис. Только тогда можно говорить о полноценном Витаукте.
Итог, полный Витаукт возможен только в условиях переподчинения сенесцента ювентальности и доминирования последнего, что ведёт к восстановлению функций в высших штабах регулировок: тимусе, эпифизе, гипоталамусе. Для этого в первую очередь нужен возврат эдафических градиентов в исходное состояние.
Итак, начинать надо с подзарядки клеток Жизненной Силой. Подзарядка живого жизнью аналогично тому как подзаряжают минусовыми «живыми» зарядами пищевые продукты. Например, для этого предлагается пищевой продукт (допустим суп, сок, оживлённые яйца без скорлупы) поместить в токопроводную ёмкость, например тонкий п/э стаканчик (или кулёчек) и разместить его в ёмкость с другой жидкостью, водой. Через электроды прибора «живой и мертвой воды» заряжаем эту воду. Заряды из внешней ёмкости через стенки стаканчика попадут на раствор в стакане и продукт в нём. Через несколько часов минусовой заряд равномерно распределится по всему объёму продукта. Точно также действует и парабиогенный эффект, когда мы нашему телу передаём среду USAP, например от пробужденных в инкубаторе яиц, проростков с корнями семян горошка, чечевицы и др., измельченных до консистенции смузи. Всё это проводить на фоне ограничения калорийности и интервального голодания для запуска аутофагии. При регулярном и длительном применении такой пищи среда USAP начнёт доминировать над SASP, что и запустит процессы ювентализации. Кроме того, можно усилить эффект от применения живой ювенильной пищи путём дополнительной её подзарядки как это описано выше со стаканчиком с помощью прибора «Живая и мёртвая» вода. Также важен комплекс препаратов по оживлению тимуса и эпифиза. Этому же будет способствовать и процедуры с применением красного ближнего света, что оживит митохондрии. Всё это вместе взятое окажет воздействие на смену эпигенетической среды клеток (смена эдафотопов*) и будет активировать нужные процессы в эпигеноме (смена эпигенотопов*, то есть совокупности паттернов, которые проявляют тот или иной модификат) путём выравнивания нужного баланса между процессами метилирования и ацетилирования, заставляя их вернуться в исходное состояние ювентальности. Как известно, сенесцент связывают с гиперметелированием и задача достигнуть деметилирования.
Конечно, может возникнуть резонный вопрос почему такого эффекта пролонгированной ювентальности нет в культуре ткани, где у юных куриных фибробластов неизменно проявляется лимит Хейфлика? Автор этому явлению дал в своих книгах трактовку и считает, что здесь заложена не программа на старение, а его вызывает новый контекст содержания клеток животного типа вне организма.
Термины
- Адальтус — этап онтогенеза, когда проявляется максимальная генеративная зрелость. У людей 25–45 лет.
- Актиноритмы — это суточное чередование света и темноты. В процессе длительной эволюции все живые организмы приспособились к определённым суточным ритмам лучистой энергии. В организме человека изменение актиноритмов (соотношения длины дня и ночи) может влиять на внутренние механизмы. Например, увеличение длины дня и светового потока возбуждает организм и истощает его, а ограничение света, наоборот, может быть профилактическим средством от некоторых болезней.
- Анизомодусы — каждое из возрастных состояний клеток (фенотипов) имеет свой статус паттернов, свою зафиксированную эпи- надпрограмму, которая поддерживает свой анизомалийный гомеостаз = анизомодус (ущербный или вредоносный). — Термин предложил Г. А. Гарбузов.
- Анизо-паттерны — патологически изменённый комплекс гистонов на ДНК. — Термин предложил Г. А. Гарбузов.
- Анизостаз — выход из прежних оптимальных рамок данного гомеостаза и появление нового устойчивого состояния на основе новой анизоконстанты. — Термин предложил Г. А. Гарбузов.
- Анизопения — процесс, сопряженный с сенесцентом и резистентностью клеток, но с привязкой к конкретному типу ткани, например, меланопения связана с функциональной недостаточностью стволовых клеток меланоцитов, что проявляется в поседении волос; тимопения связана с недостаточностью стволовых клеток тимуса; пинеалопения — недостаток стволовых клеток и ослабление функций эпифиза; ретинопения; остеопения… — Термин предложил Г. А. Гарбузов.
- Анизомалия — неадекватные для Витаукта параметры жизнедеятельности, которые находятся за пределами коридора гормезиса и ведут к неизбежным особым состояниям. Они накапливаются с возрастом. Автор предлагает отличать понятие «анизомалия» от понятия «возраст-ассоциированные заболевания», так как возрастные нозологии могут иметь двойственное состояние. Примером чётко объясняющим эту разницу является диабет II, который в раннем возрасте его следует признавать возраст-ассоциированным заболеванием (преждевременным), так как доля патогенных начал здесь преобладает, а значимость сенесцента невелика; тогда как в глубокой старости в связи с нарастанием всеобщей резистентности (инсулинорезистентности в частности) и уровнем сенесцента только нарастает и рано или поздно эта скрытая резистентность обязательно проявится в виде той или иной анизомалии (например, диабета). В этом случае он переходит в категорию анизомалий – неизбежных возрастных проявлений (манифестаций). Таким образом, следует различать возраст-ассоциированные заболевания от анизомалий, так как методики их преодоления различные. Итак, при болезнях и возраст-ассоциированных заболеваниях (наличие компоненты сенесцента) обязательно следует обращать внимание на конкретные механизмы патологии и локальное воздействие на них, что абсолютно не подходит при анизомалиях, то есть возрастных перестройках, связанных как с сенесцентом, так и сенилитом всего организма, при которых в первую очередь нужны совершенно другие методы, в частности общего омоложения и оздоровления организма (повышения жизненной силы, противодействующей сенесценту) и укрепления его Витаукта (противодействующего сенилиту), иначе все остальные частные методики будут неэффективны. Анизо — перекос, несоответствие, «малия» — часть от слова «аномалия», то есть отклонение от нормы. — Термин предложил Г. А. Гарбузов.
- Гено-ювентал — регулировка клеточной молодости со стороны программ генома. — термин предложил Г. А. Гарбузов.
- Геронтос — общее старение регулируется одновременно двумя рычагами на двух этажах: на нижнем уровне фенотипа клеток (сенесцент) и на верхнем уровне всего организма в виде онтофизисных фенотипов (сенилит). — Термин предложил Г. А. Гарбузов.
- Гормезис — интегрированный свод гомеостазов, задающий коридор оптимума для проявления жизнедеятельности в живой системе, который имеет верхние и нижние границы регулировки, где каждая граница имеет свои механизмы, обеспечиваемые противоположными генными программами: центральные параметры регулируют транспозиты, а крайние пограничные — контрпозиты. — Термины предложены Г. А. Гарбузовым. — Следует выделять понятия Большой Гормезис — интегральный свод механизмов, которые определяют предел, границы возможностей динамики онтогенеза организма, в том числе при выходе его за рамки Великого Гормезиса, ведущего к сенилиту, который тоже реализуется через механизмы гипоталамуса, а также малый гормезис = просто гормезис, то есть интегральная возможность противостоять всем внешним стрессовым факторам, которые откладывают свой отпечаток на темпы старения гипоталамуса. Но это влияние не превышает возможности Большого Гормезиса. — Понятия ввёл Г. А. Гарбузов.
- Гомеорез — механизмы возрастного смещения параметров гомеостаза.
- Гормезисорез — механизмы возрастного смещения параметров гормезиса.
- Гомойотопия — ограниченность роста, от слова «гомойо» — способность всех особей вида или органов в них достигать жёстко заданных величин, например, размеров, а «топо» — от слова «топология» — размеры, пространство. — Термин предложил Г. А. Гарбузов.
- Гомеостазорез = гомеорез — механизмы возрастного смещения параметров гомеостаза. — Термин предложил Г. А. Гарбузов.
- Кейлонный механизм регулировки — первично инициирующее программируемое изнутри клетки звено регуляции клеточного гомеостаза тканей, которое происходит за счёт перестройки и изменения ДНК в некоторых генах и обеспечивающее контроль над процессами модификаций (или фенотипов, или субпопуляций) и размножения клеток.
- КРП — клетки регуляторы пролифераций - по сути, это иммунные клетки, в т.ч. Т-лимфоциты, макрофаги или клетки-резиденты, регулирующие рост или ограничение его у стем-клеток.
- Матура — этап онтогенеза, перезрелости, климакса с выходом за пределы, границы оптимума коридора гормезиса, предшествующий сенилиту. — Биологический смысл этого термина ввёл Г. А. Гарбузов.
- Метавоспаление — от слов «за», «после» означает, что оно появляется в клетках, вышедших за рамки оптимума, за рамки гомеостаза. При этом они выделяют сигналы SOS (интерлейкины, интерфероны…), но чаще всего это запрограммированный естественный процесс перемодификации клеток, ответ или подстройки к новым условиям и внешним требованиям растущего или меняющегося организма. Это форма эндогенной природы хронического воспаления, вызванного хроническим метаболическим дисбалансом, например, в связи с входом сенесцентных клеток в режим неоптимальных гомеостазов или гликолиза. Отличается от термина провоспаление, которое может быть вызвано также и внешними неинфекционными факторами. Автор ввёл своё понимание термина метавоспаление - это следствие процесса сенесцента клеток, которое происходит кейлонным способом, то есть путём автономного старения популяции клеток, а значит исходящего изнутри клеток. В свою очередь провоспаления наводятся клетками уже ставшими сенесцентными за счёт выделения своего секретома.
- Модификаты — невозвратное изменение макрофагов и иных иммунных клеток в условиях приспособления клеток к эндогенным перестройкам и изнутри исходящего секретома. — Термин предложил Г. А. Гарбузов.
- Неотения — способность организма продлевать свои ювенильные этапы существования и тем самым продлевать жизнь.
- ОАС — Общий Адаптационный Синдром по Г. Селье.
- Онтофизис — у растений подразумевает не простое закрепление у клонов неких особенностей роста и плодоношения, а проявление более общего процесса, то есть сохранения степени онтостадийной зрелости, в том числе и высшей её степени, когда полностью заблокированы рост или плодоношение на нижних побегах. Но блокировка происходит не на уровне генов, а на уровне сложившегося комплекса активности камбиальной ткани и соответствующей ей стромы. В отличие от высшей степени проявления онтофизиса у побегов растений, в животном мире аналогом этому является сенесцент у клеток. Онтофизис = сенесценту. Разблокировать такое состояние у растений возможно только при особых условиях реювенилизации, то есть снятии апикального доминирования, и обязательном превалировании цитокининового фона. При этом расширено понимание данного явления не только для клонов, но и в пределах данной особи растения, когда новое поколение побегов в пределах одного и того же дерева проявляет продвинутую физиологическую или морфологическую стадийную зрелость. Программы на ювенильность у них заблокированы. Онтофизис в животном мире подразумевает образование множественного разнообразия возрастных фенотипов клеток. Это в свою очередь откладывает свой отпечаток, отражение на возрастных этапах в виде качественных изменений во всех структурах организма. Фенотипия (не путать с морфотипами) клеток определяет онтофизис на уровне тканей. Набор определённой критической массы переходов по фенотипическим ступеням определяет становление сенесцента. Причем такая возможность сенесцента заранее предусмотрена эволюционно для клеток животных. Это и есть механизм коммитации, то есть перехода на сенесцент. Кроме морфотипической динамики в тканях и органах с возрастом происходят (накладываются) онтофизисные процессы. Они основаны на динамике соотношения ювентальных/сенесцентных клеток, доминирования того или иного типа их фенотипов. Морфо- и фенотипы в совокупности в масштабах всего организма отображают этапы онтогенеза (детство, юность, адальтус, матура, сенилит). При этом фенотипы клеток отображают изменчивые модификаты и трансформаты для некоторых морфотипов. Фенотипы накладываются на морфотипы, которые могут быть представлены рядом фенотипов. Точнее, когда фенотипы сенесцента становятся доминирующими над ювентальными, они запускают усиление проявления фенотипов онтофизиса в тканях и органах; в том числе это является причиной возрастных перестроек в интегрирующих всё «штабах» регулировок, включая элевацию в одних и инволюцию в других. Это и является механизмом реализации становления (через ступени на онтодианной линии). При пересадке старых органов молодым особям это их состояние старости отражается на организме-акцепторе. То есть это закрепление неких возрастных (фенотипических на уровне эпигенома) и онтогенетических перестроек (морфотипических, на уровне генов), которые сохраняются и у линий клеток в культуре ткани, аналогично тому, как это сохранение происходит и у клоновых потомств в виде топофизиса (особенностей роста побегов: ортотропного /прямоствольность/ или плагиотропного /рост в бок/), или циклофизиса (способность к закладке или не закладке тех или иных генеративных органов), или онтофизиса (с сохранением темпов клеточного роста или самообновления, либо их полной блокировки). Особенностью клеток животного типа является то, что до сих пор не найден гормон реювентализации сенесцентных клеток, а значит и онтофизисных тканей, что и является причиной «непреодолимости» лимита Хейфлика. При этом особенностью выращивания клеток в культуре ткани является быстрый «перескок» через все онтостадии и остановка на крайней онтофизисной стадии. — Термин предложил Г. А. Гарбузов.
- Онтодианная линия жизни, онтодианность, онтодиана, фенотипическая онтодианность — показатели длительности онтогенеза, на которую рассчитан данный вид, исчисляемый в годах. Как в растительном, так и животном мире имеются виды, где одни из них проявляют короткожительство, а другие — долгожительство, которое обеспечено у каждого конкретного вида своим механизмом регулировки онтогенеза (через взаимодействие сенесцента и сенилита). Это означает, что у каждого вида длительность жизни изначально коммитирована, то есть генетически запрограммирована. Термин создан по аналогии с циркадианностью, когда ритмы жизни связаны не с внешними факторами, а с внутренними. — Термин предложил Г. А. Гарбузов.
- Парабиогенез, парабиогенный эффект — от слов «биогенез», которое в эмпирическом обобщении означает стимулирование живого организма, а точнее когда одно живое активирует, оживляет другое, где «пара» (дословно — рядом, около) означает, что активация происходит за счёт живого начала, но не близковидового происхождения. — Термин предложил Г. А. Гарбузов.
- Пубертат — этап онтогенеза, когда наступает половозрелость.
- Сенилит — старение на общеорганизменном уровне.
- Сенесцент — старение на клеточном ровне.
- Сенолитик — вещества способные растворять старые клетки.
- Стем-клетки — недифференцированные биологические клетки, которые могут дифференцироваться в функциональные.
- УКАМ — Универсальный Клеточно-тканевой Адаптационный Модус – пролог для сенесцента.
- Трансформаты — в отличие от фенотипов (возвратное изменение макрофагов и иных иммунных клеток в условиях их реакции на внешние факторы) и модификатов (невозвратное изменение макрофагов и иных иммунных клеток в условиях приспособления клеток к эндогенным перестройкам и изнутри исходящего секретома), трансформаты — это когда процесс с иммунных клеток-резидентов и других клеток-менеджеров переходит на стем-клетки с последующими дегенеративными процессами. — Термин предложил Г. А. Гарбузов. Начинается процесс с иммунных клеток, но переходит на все клетки данного вида ткани. Так стареет постепенно вся ткань. Возрождение, омоложение ткани возможно только с восстановления модификатов иммунных клеток.
- Феноптоз — механизмы, обеспечивающие неизбежное отмирание субъектов вида.
- Эдафическая среда, эдафотоп — от греч. слова эдаф – основание, земля, почва и топ - место. — Гарбузов Г.А. выдвинул концепцию, что каждый тип модификаций клеток (ювентальный или сенесцентный) генетически или эпигенетически настроен на свой эдафотоп, который обусловлен преобладанием SASP или USAP секретома.
- Эмитент — дословно дающий указания-регламент развития. Тимус можно условно (после его иммунных обязанностей) также назвать и органом эмитентом (банком), то есть раздающим важную информацию предписаний (указания-«ценные облигации-дотации» для реализации), то есть направления того или иного пути развития (юность–зрелость), тогда как эпифиз является для него первым органом-эмиссаром, который воспринимает эти указания и их диверсифицирует (преобразует, переводит на другой язык) для дальнейшего осуществления. – Биологическую трактовку этого термина предложил Гарбузов Г.А.
- Энергоанизостаз — энергонедостаточность, аномальная энергетика сенесцентных и онкологических клеток, основанная на гликолизе. — Термин предложил Г. А. Гарбузов.
- Эпигенотоп — совокупность активных паттернов эпигенома, которые проявляют тот или иной модификат клетки, что обеспечивается путём выравнивания соответствующего баланса между процессами метилирования и ацетилирования, заставляя их вернуться в исходное состояние ювентальности. — Термин предложил Г. А. Гарбузов.
- Эпигенез — это когда вновь приобретённые особенности клеток и тканей связаны не с морфогенезом за счёт генопрограмм, а базируются на эпигенетическом уровне. Эпигеномный уровень — основа для фенотипов, модификатов, сенесцента, которые тоже реализуются через эпигенез и тоже сцеплены с тем же блоком генов. В отличие от обычных иммунных фенотипов (М1, М2…), при сенесценте эта фенотипия переходит в устойчивую модификацию (невозвратную, то есть изменения происходят в большей степени не со стороны функциональных возможностей, а структурно). Это уже фаза не просто активации, а гиперактивации иммунных клеток. В этом режиме они выходят за рамки гомеостазов, становятся резистентными, не подчиняемыми (сенесцентными). Фенотипические изменения переходят в модификационные.
- Эпи-ювентил — механизм регулировки ювентальности клетки со стороны эпигенома в двухэтажном механизме поддержки ювентоса (клеточной ювентальности). — термин предложил Г. А. Гарбузов.
- Ювентал, ювентальные клетки — состояние молодости, относящееся сугубо к клеточному уровню. Термин введен с целью различения от понятия ювенильность, то есть молодости всего организма на основе особого иммунного статуса и гормонального фона. Механизмы реализации этих процессов разные и происходят на разных уровнях. Ювентальные клетки не имеют блокировки ряда генов сенесцента, или точнее, сенесцентные клетки заблокировали гены ювентальности. Речь идёт об антисенесцентных генах (антисенесценция) и о генах ювентальности и сенесцента (коммитирующих генах). При этом ювентальные клетки обладают ювентальными эпигенетическими паттернами, тогда как у сенесцентных клеток эти паттерны сенесцентные, а у онкологических – свои онкологические паттерны – свои гистоновые надстройки. — Термин предложил Г. А. Гарбузов.
- Ювентальный реверс — возможность клеток (или даже целиком особей, например, медузы) в тканях возвращаться из зрелых и сенесцентных клеток в исходное стволовое состояние с преодолением лимита Хейфлика, а также проявлять обратный метаморфоз в ювенильное состояние на основе механизма возврата клеток из фенотипа сенесцентных в нормальные — термин предложил Г. А. Гарбузов. Таким образом можно говорить о реверсе Гарбузова как противоположность лимиту Хейфлика. Термин связан с понятием ювентальные клетки, ювентальность и понимает состояние клеток, противоположное сенесценту, в отличие от термина ювенильность, то есть молодости всего организма на основе особого иммунного статуса и гормонального фона. Ювентальные клетки имеют разблокировку от генов сенесцента, или наоборот, сенесцентные клетки заблокировали гены ювентальности. Речь идёт об антисенесцентных генах (антисенесценция) и о генах ювентальности и сенесцента (коммитирующих генах). Лимит Хейфлика и реверс Гарбузова – два противоположных фенотипа, основанные на механизмах ювентальности и сенесцента.
- ATG — комплекс генов, регулирующих аутофагию.
- SASP — стареющие клетки выделяют множество факторов, которые называют «секреторным фенотипом, ассоциированным со старением»; является антиподом UASP.
- UASP — это так называемый «секреторный фенотип, ассоциированный с ювентальностью» (понятие предложил Гарбузов Г. А.). Ювентальные клетки выделяют множество специфичных факторов ювентально-ассоциированного спектра секретома, на которых держится гомеостаз фенотипа ювентальности. Альтернативное состояние модификатов (фенотипов), когда вырабатывается SASP, то есть сенесцентно-ассоциированный спектр секретома.
Литература
- Мун Валерий. Старость — упущение иммунной системы или ее предательство?
- Житова Дарина. Ученые выяснили, что удаление тимуса повышает риск смерти почти в 3 раза.
- Трине Х. Попперуд. Тимэктомия при ювенильной миастении безопасна с точки зрения долгосрочных иммунологических последствий.
- Донцов В. И. Регуляция лимфоцитами клеточного роста соматических тканей и новая иммунная теория старения. 1998
- Линькова Н. С. Иммунные клетки эпифиза при его старении.
- Melissa S. Ventevogel, Gregory D. Sempowski. (2013). Thymic rejuvenation and aging. Current Opinion in Immunology. 25, 516–522.
- Melissa S Ventevogel, Gregory D Sempowski. (2013). Thymic rejuvenation and aging. Current Opinion in Immunology. 25, 516–522.
- Арушанян Э.Б., Бейер Э.В. Мелатонин: биология, фармакология, клиника.
- bspu.by/blog/pugachvalentin/article/lection/… Лекция. Структурно-функциональные особенности эндокринной системы детей и подростков.
- Эпиталон и эпифиз // «Russian Peptide».
- Черник В.Ф. Возрастная физиология: лекция 3.
- Сукальская Анастасия, Старокадомский Петр. Наивные Т-клетки — ключ к долголетию.
- Franceschi et al., 2000. One of the main characteristics of aging is chronic activation of the immune system that results in low-grade inflammation, which is mainly driven by macrophages.
- Bruunsgaard, 2006; Maggio et al., 2006. The mediators of this systemic inflammation are pro-inflammatory cytokines such as interleukin-6 and tumor necrosis factor alpha, which increase with increasing age.
- Coppe et al., 2008; Freund et al., 2010. The SASP includes growth factors, proinflammatory cytokines, chemokines, and proteases, all of which can contribute to inflammaging.
- Гарбузов Г. А. Актиноритмическое лечение онкологии (Книга. Электронная версия). // garbuzov.org.
- Гарбузов Г. А. Неотения — продлённая молодость. Можно ли её сохранять неограниченно с помощью аутофагии? // garbuzov.org.
- Вирна Маргарита, Хименес Мартин. Мелатонин как средство против старения при возрастных сердечно-сосудистых и нейродегенеративных заболеваниях.
- Гарбузов Г. А. Эпифиз — верховный драйвер онтогенеза. Ключ к молодости и здоровью.
- Мэн-Мэн Сюй. Мелатонин улучшает состояние при остром обострении ХОБЛ, вызванном вирусом гриппа, подавляя поляризацию макрофагов M1 и апоптоз.
- Лузикова Е. М. Влияние мелатонина на макрофаги и клетки дисперсной эндокринной системы селезёнки.
- Shivali. Scientists have uncovered a simple way to banish grey hairs.
- Tae-Won Kang, Tetyana Yevsa, Norman Woller, Lisa Hoenicke, Torsten Wuestefeld, et. al. (2011). Senescence surveillance of pre-malignant hepatocytes limits liver cancer development. Nature. 479, 547–551.
- Дильман В. М. Почему наступает смерть. 1972.
- Гарбузов Г. А. Единство иммунных механизмов реализации старения клеток (сенесцент), старения организма (сенилит) и онкологии.
- Ян Лю. Метаболическое перепрограммирование в реакциях макрофагов.
- Гарбузов Г. А. Как продлить молодость? Серия: Биология молодости. Кн. 2 // garbuzov.org.
- Гарбузов Г. А. Возможности дихлорацетата в роли сенолитика…
- Национальный университет Сингапура. «Скрытая сила ДНК может изменить подход к производству лекарств». ScienceDaily.
- Учёные обнаружили «разделение труда» в митохондриях. Science news, 8 Nov., 2024
- Metabolism Journal: Propagation of senescent phenotypes by extracellular HMGB1 is dependent on its redox state.
Книги автора
 ЭПИФИЗ — ВЕРХОВНЫЙ ДРАЙВЕР ОНТОГЕНЕЗА. КЛЮЧ К МОЛОДОСТИ И СТАРЕНИЮ
ЭПИФИЗ — ВЕРХОВНЫЙ ДРАЙВЕР ОНТОГЕНЕЗА. КЛЮЧ К МОЛОДОСТИ И СТАРЕНИЮ
Старение — это многоуровневый процесс как на верхних этажах регулировок (системном), так и на нижнем клеточном. Чтобы адресно разрабатывать методы противодействия и сдерживания общего потока старения (геронтос), необходимо найти правильный ответ — откуда исходят именно истинные первичные начала этого общего процесса. Автор провел глубокий анализ природы старения как в растительном мире, так и в животном. Показано, что этот процесс является двусторонним: снизу он исходит с уровня клеток (сенесцент), причиной является эпигенетическая коммитация на основе онтофизиса; а сверху верховным драйвером этого процесса является эпифиз, а не гипоталамус, как это считалось ранее. Исходя из этих фундаментальных разработок, предложен комплекс методик воздействия на все уровни сдерживания старения. Показана динамика взаимовлияния друг на друга верхнего и нижнего этажей старения. Именно верхний этаж определяет весь спектр возрастзависимых заболеваний (анизомалий). Если мы научимся сохранять «эпифизарную молодость» = неотению, то отодвинем старость.
 ВЗЛОМ ИММУННЫХ МЕХАНИЗМОВ СТАРЕНИЯ — ПУТЬ К ЮНОСТИ И ЗДОРОВЬЮ
ВЗЛОМ ИММУННЫХ МЕХАНИЗМОВ СТАРЕНИЯ — ПУТЬ К ЮНОСТИ И ЗДОРОВЬЮ
Эта книга знакомит читателя с принципами и методиками противодействия старению. Автор впервые разработал интегральную теорию старения организма, которая рассматривает его в виде взаимодействия двухуровневого процесса как на уровне клеток (сенесцент), так и на уровне всего организма (сенилит). Ознакомившись с материалами, приведёнными в данной книге, вы поймёте, что надо делать, чтобы как можно дольше сохранять молодость, здоровье и бодрость духа.
 ЗДОРОВЬЕ, МОЛОДОСТЬ, ДОЛГОЛЕТИЕ. КАК МАГНИЙ И ОКСИД АЗОТА ПРОТИВОСТОЯТ СТАРЕНИЮ
ЗДОРОВЬЕ, МОЛОДОСТЬ, ДОЛГОЛЕТИЕ. КАК МАГНИЙ И ОКСИД АЗОТА ПРОТИВОСТОЯТ СТАРЕНИЮ
Глубокий анализ существующих причин старения позволил автору создать свою единую теорию «биологии старения», которая строится на интеграции процессов сенесцента (на уровне клеток) и сенилита (на системном уровне). Показана решающая роль магния и оксида азота в регулировке на клеточном уровне сенесцента. Именно сенесцент (нарушение гомеостазов) определяет механизм сенилита (нарушение гормезиса и витаукта), а с ними и возрастзависимых «болезней», которые на самом деле не болезни, а естественные анизомалии, то есть механизмы реализации старения. Только правильное понимание сути природы старения позволит выйти на правильные пути преодоления возрастных болезней и продления жизни человека через механизмы неотении (продлённой молодости), чему посвящена следующая книга автора «Биология молодости».
 САМОУНИЧТОЖЕНИЕ РАКОВЫХ ОПУХОЛЕЙ. ФЕНОМЕН АПОПТОЗА
САМОУНИЧТОЖЕНИЕ РАКОВЫХ ОПУХОЛЕЙ. ФЕНОМЕН АПОПТОЗА
Книги можно заказать на сайте garbuzov.org.
Онкология. Можно ли её вылечить безвредными способами? Автор впервые показывает, что можно и нужно! Для этого нужно запустить механизмы избирательного самоуничтожения раковых клеток в организме на основе клеточных программ апоптоза и аутофагии, которые нужно адресно открыть. Предложена Комплексная Программа из противоположно направленных методов, вычлененных в две фазы и направленных на расшатывание и перебалансировку основных жизнеобеспечивающих механизмов клеток, в т. ч. антиоксидантной « прооксидантной, провоспалительной « антивоспалительной и др. У онкоклеток коридор возможностей самозащиты, их гормезис намного уже, чем у нормальных клеток, у которых Жизненная Сила, Витаукт, намного выше. Такая разность возможностей позволяет создавать особые условия, когда становится возможным запуск механизмов самовыбраковки онкоклеток.
 БИОЛОГИЯ МОЛОДОСТИ – электронная рукопись 2026 г
БИОЛОГИЯ МОЛОДОСТИ – электронная рукопись 2026 г
Ознакомиться с ней можно на сайте garbuzov.org.
Практически все авторы научно-популярных работ по анти-эйдж теме рассматривают всевозможные методы сдерживания старения и продления жизни, здоровья… Автор книги впервые показывает, что это не эффективно, так как не убирает суть проблемы и связывает эту тему через продление молодости, которая и есть фундамент для всего остального. Без продления молодости невозможно радикального решения всех остальных проблем. Автор подробно анализирует биологию молодости, объясняет почему она уходит. Важнейшими для запуска старения являются механизмы неспецифического иммунитета, а также старение клеток (сенесцент). Изучен весь мировой опыт и знания по продлению молодости на всех уровнях организма, что автоматически отодвинет все «болезни» старости - анизомалии.
Книгу или Программу-консультацию по заболеваниям Вы можете приобрести по нашему адресу.
Вы можете обратиться с вопросами или за консультацией к Гарбузову Геннадию Алексеевичу на сайте garbuzov.org, по адресу: vitauct@yandex.ru или по телефону 8 (928) 239-13-64.

Биолог, дипломированный фитотерапевт, нутрициолог, кандидат биологических наук
Стаж 40 лет
Подробнее обо мне