Средний срок доставки от 2 до 6 дней
АННОТАЦИЯ
Практически все авторы научных или популярных работ по анти-эйдж теме рассматривают всевозможные методы сдерживания старения и продления жизни, здоровья… Автор книги впервые показывает, что это неэффективно, так как не убирает суть проблемы и связывает эту тему через продление молодости, которая и есть фундамент для всего остального. Без продления молодости невозможно радикального решения всех остальных проблем. Автор подробно анализирует биологию молодости, объясняет, почему она уходит. Важнейшими для запуска старения являются механизмы неспецифического иммунитета, а также старение клеток (сенесцент). Изучен весь мировой опыт и знания по продлению молодости на всех уровнях организма, что автоматически отодвинет все «болезни» старости — анизомалии.
О книге
До сих пор научный мир не может дать окончательный точный ответ, откуда берут начало механизмы старения организма. Существует масса разрозненных теорий, не позволяющих дать ответ для разработки реальных методов радикального продления жизни. Глубокий аналитический поиск и практика позволили выйти автору на новый уровень понимания глубин этой проблемы. Разработана интегральная теория старения организма (геронтос), которая рассматривает его в виде взаимодействия двухуровневого процесса как на уровне клеток (сенесцент), так и на уровне всего организма (сенилит). Первично сенесцент запускается как элемент возрастного морфогенеза для реализации локальных инволюций в высших центрах регулировок. В этих «штабах» имеется система резидентных иммунных клеток, особо чувствительных и реагирующих первыми на динамику изменений в системе. Часть из этих клеток является представителем врождённого «тренируемого» (неспецифического) иммунитета. Зарождаются они в тимусе кейлонным путём (самопровоцируемая коммитация), а затем процесс оттуда распространяется как «снежный ком» на другие «штабы регулировок», в которых тоже есть иммунные сенсоры (в ювентальном статусе). Одни из них способны реагировать на динамику изменений в системе путём запуска, образования, с одной стороны, эпигеномных модификаций (повышение функциональности и дифференциации), а с другой — сенесцентных линий клеток, а на определённом этапе изменений сенесцентные клетки начинают доминировать над ювентальными.
В иммунной системе имеется часть клеток (субпопуляций), которые отвечают не за иммунные вопросы, или трофику ткани, а за онтогегенетические трансформации этих тканей. При этом они являются представителями врождённого «тренируемого» (неспецифического) иммунитета.
Так, известны научные разработки, которые показывают роль особой субпопуляции Т-лимфоцитов, которая участвует именно в составе сингенной* смешанной культуре лимфоцитов для поддержания нужного уровня клеточного роста и обновления в организме. Это важно для понимания того, что рост стволовых клеток и их ювентальность регулируется через иммунную систему (в т. ч. и клеток-резидентов, и Т-лимфоцитов) и зависит от роли снижения её численности и активности в функции для старения. В этом суть новой иммунной теории старения. На фоне вырождения лимфоидных тканей и со старением этой субпопуляции Т-лимфоцитов и макрофагов-резидентов происходит и сенесцент клеток, в том числе стем-клеток*. Следовательно, ювентальность может поддерживаться через сингенность, и этим следует уметь воспользоваться.
Процесс фиксируется эпигеномно появлением новых клеточных фенотипов и модификатов. Они же через свой секретом «заражают» сенесцентом, трансформируют рабочие и стволовые клетки, локальные ткани. Это является прологом к инволюционным процессам в них из-за повышения резистентности. В итоге данный «штаб» утрачивает свою доминантную роль, инволюционирует с ослаблением функциональности и повышением резистентности. Это является первичным механизмом переключения с одного «центра регулировок» на другой, что позволяет переходу с одного этапа онтогенеза на следующий. При этом разблокируются и элевационируют нижестоящие звенья «штабов», переводя их в статус доминантности. В них также через иммунные клетки запускаются механизмы сенесцента, провоспаления и инволюция. Первым сенесцентирует тимус (обеспечивает этап детства), затем эпифиз (этап юности), гипоталамус (зрелости), железы-мишени и ткани (сенелит)… Так происходят продвижения их по онтодианной линии, где окончательная сумма этих изменений является геронтосом. Повышение резистентности и сенесцента в верховных штабах по системе обратной связи распространяется на железы-мишени, органы, ткани через иммунные клетки-резиденты… Здесь статус сенесцента масштабируется и эскалируется за счёт многократного усиления выброса факторов сенесцента. Это становится причиной обратного эшелона сигналов снизу наверх, что многократно усиливает сенесцент в верхних штабах и становится причиной генерализации (экстернализации) и резкого усиления инволюций и сенилита. Как итог Гормезис (гармония гомеостазов) такой системы выходит за пределы Витаукта и переходит в Энтроукт (кокафония гомеостазов), что является неизбежным условием возраст-зависимых «болезней» (анизомалий). Такое понимание проблемы позволило автору осознать принципы по противодействию геронтосу на основе деэлевации и деэскалации для антисенесцента и антисенилита.
Двухъярусная регулировка старения, Или геронтос = сенесцент + сенилит
Сенесцент и сенилит базируются на неспецифической стороне проявлений, присущей для всех болезней и анизомалий*
Старение, или геронтос, — это двухэтажный процесс, состоящий из взаимодействия сенесцента* и сенилита*
При этом каждый из них вовлекает в свою орбиту противоположный уровень. Динамика каждого из них ориентируется на статус противоположного, они сопряжены. Делается это ступенчато, когда одна из двух сторон процесса индуцирует другую (на другом этаже регулировок), а та впоследствии усугубляет глубину изменений в противоположной стороне. В итоге процесс развивается ступенчато, по этапам, что проявляется в виде различных этапов онтогенеза, или Онтодианной Линии Жизни:
фетос* ↔ ювентос* ↔ адальтус* ↔ матура* ↔ геронтос ↔ мортус ⊣ феноптоз ∤.
У каждой ступеньки есть свой порог возможностей, запас прочности, при выходе из которого запускается следующая ступень. Все этапы укладываются последовательно, в сумме представляют Онтодианную Линию Жизни*. Причём у каждого вида имеется своя (обозначенная генами) длина хроноса для этой линии. Геронтос = сенесцент + сенилит, то есть является реализацией взаимоусиления этих двух процессов. При этом сенилит работает на уровне механизмов гормезиса*, а сенесцент — на уровне регулировок гомеостазов. Гормезис обеспечивает Витаукт* на уровне организма, а гомеостазы обеспечивают Жизненную Силу* на уровне клеток. Витаукт зависит от Жизненной Силы, и наоборот, ⇄ Жизненная Сила зависит от Витаукт. У Витаукта и Жизненной Силы имеются свои механизмы регулировок на верхнем и нижнем этажах организма. При этом сенесцент означает утрату Жизненной Силы, а сенилит — Витаукта. Идеальным является, когда эти динамические потоки саморегулировок стабилизированы на каждом этаже, не меняются, что обеспечивает потенциал непрерывного существования у каждого. Например, растительные клетки способны производить деления неограниченно, а вегетативные клоны тоже способны поддерживать нелимитированное существование.
В чём суть сенилита? Он вовлекает некоторые (включая иммунные, нейрогенные, гормональные…) элементы ОАС (Общий Адаптационный Синдром).
В чём суть сенесцента? Он вовлекает УКАМ (Универсальный Клеточно-тканевой Адаптационный Модус). Причём в отличие от морфогенеза (регулируется генами путём транскрипции РНК и белков) сенесцент регулируется надгеномно, через механизмы эпигенеза, который в свою очередь сопряжён с динамикой сенилитных процессов. Таким образом, сенесцент и сенилит определяют друг друга.
Чем отличается геронтос от сенилита? Геронтос также реализуется через сумму ОАС и УКАМ, но в отличие от них закрепляет эти статусы на уровне гомеостазов и гормезиса посредством механизмов эпигенеза и инволюций. При этом УКАМ здесь работает в другом формате, на принципах, когда клетки находятся на стадии IV, истощения. Это уже не ситуационные фенотипы, а устойчивые модификаты. Такие клетки, как штрейкбрехеры (предатели), работают в противоположном направлении или недорабатывают полноценно. Это действие происходит в первую очередь через клетки местного иммунитета, которые образуют устойчивые новые модификаты*.
Роль иммунных клеток в созревании эпифиза и его старении
Это представление совпадает с новой иммунной теорией старения [1], в которой рассматривается регуляция лимфоцитами клеточного роста соматических тканей. Анализ показывает, что возможность саморегуляции ткани осуществляется специализированными клеточными популяциями, выполняющими функцию межклеточной регуляции роста разнотипных соматических тканей. Считается, что такая система может быть представлена специализированными Т-лимфоидными клетками. Снижение функции таких регуляторных клеток с возрастом может являться центральным механизмом для старения самообновляющихся соматических тканей организма и определять снижение с возрастом ростового потенциала тканей старого организма.
Предложены представления о КЕЙЛОННОЙ системе саморегуляции, работающей для одной клеточной популяции. Таким образом, отдельные ткани эпифиза развиваются как по своим правилам роста и его ограничений, так и отвечают на сигналы сенесцента из тимуса, что приводит к их функциональным ограничениям. Таким образом эпифиз регулируется как снизу и сверху, то есть за счёт своих внутренних возможностей, так и корректируется (подавляется) со стороны тимуса.
Что такое гомеостаз ткани?
Микроглиоциты встречаются в паренхиме эпифиза среди гормон-синтезирующих клеток пинеалоцитов. Получены данные, свидетельствующие об участии микроглиальных клеток (разновидность иммунных, образующихся из примитивных макрофагов и попадающих в мозг в процессе кровообращения) в развитии воспаления в эпифизе человека в ходе старения [2]. Микроглия способна вырабатывать цитокины как анти-, так и провоспалительного действия. В зависимости от внешней и внутренней ситуаций происходит модификация микроглии с запуском тех или иных цитокинов, в том числе и работающих на сенесцент.
В эпифизе с возрастом практически всегда находят отложения кальцинатов, что является прямым следствием провоспаления, а значит, и сенесцента
Перестройка эпифиза происходит через сенесцент. Это активное подавление функциональных пинеалоцитов. Причём появление кальцинатов и сенесцент эпифиза начинаются в раннем юном возрасте в период становления пубертата и к 25 годам находятся в полном становлении. Нигде в головном мозге и организме нет ещё появления кальцинатов и сенесцента. Кальцинаты начнут появляться в различных органах намного в более позднем возрасте и будут проявлять провоспаления и сенесцент в них. Это означает, что глиальные клетки эпифиза настроены программно на досрочный сенесцент. Если точнее, то они более чувствительны к сенесценту, и, скорее всего, не они сами по себе запускают сенесцент, а их к этому подстёгивают сигналы из тимуса, который к этому времени ещё ранее запустил программу на инволюцию.
Последовательная череда запусков процессов сенесцента
Последовательная инволюция одних органов (тимус, эпифиз) запускает-растормаживает механизмы элевации* (наращивание мощи, усиление функций) созревания в гипоталамус-гипофизарной системе. В них имеются сенсоры, определяющие уровень гормонов и реагирующие на них путём сенесцента, но почему-то не путём апоптоза. Очевидно, в норме апоптоз подразумевает активацию замены на новые клетки, тогда как сенесцент тормозит все варианты репликаций. Ткань эпифиза медленно угасает функционально и перерождается. Здесь сенесцент происходит локально. Это означает, что сенесцент — это не тотальный процесс во всех клетках, а последовательный и регулируется с верхних этажей, а затем с достижением нужного гормонального порога распространяется и по другим тканям-мишеням.
Эпифиз — главный навигатор и драйвер онтогенеза
Следует отметить, что эти перестройки усиливаются и поддерживаются сигналами обратной связи, то есть растущим гормональным фоном. Этот фон для них является стрессом, закрывает «ворота обратного выхода», поэтому нет возврата их в исходное состояние (как это должно происходить в норме у фенотипов).
Подтверждением значимости этой обратной связи из гипоталамуса при усилении его генеративной зрелости является уникальный случай, когда из-за генетических нарушений гипоталамус не смог поднять свой гормональный уровень (этап пубертата) и поддержать инволюцию эпифиза. Так известен факт нестареющего мальчика Дениса Вашурина, у которого и произошла такая мутация, и гипоталамус не смог пойти по пути элевации, а значит, через половые гормоны дополнительно подавлять эпифиз. Такая генетическая болезнь называется гипофизарный нанизм. При этом мужчина в возрасте 32 года выглядел внешне как 14-летний школьник [3].
При возрастных перестройках эпифиза затрагиваются не только иммунные клетки, но и стем-клетки. Типичное старение-сенесцент в данной ткани, как это происходит и в любой ткани. При этом происходит перераспределение в соотношении различных путей энергетического обеспечения: начинает преобладать анаэробный гликолиз. Причём это не подлинный гликолиз, связанный с гипоксией, а псевдогликолиз, ложный, подобный эффекту Варбурга при онкологии. Это когда в среде кислорода достаточно, но сенесцентные или онкологические клетки им не пользуются. Этим механизм сенесцента схож с онкологическими перестройками. Он связан с модификацией иммунных клеток, а затем угасанием стем-клеток. Это ведёт к пинеалопении*, или пинеальной резистентности. Типичное проявление сенесцента. Но важно то, что это происходит в главном регуляторном органе (дирижёре), который и определяет геронтос. Первым геронтос разворачивается в тимусе и эпифизе, когда сенесцент и сенилит наступают одновременно. Таким образом, геронтос тоже происходит локально и затем переходит в тотальный процесс.
Ступенчатое становление сенесцента в эпифизе
Из этого следует, что сенесцент — это наведённый, запускаемый последовательно процесс. Опосредуется он через онтофизис* и эпигенез. Сенесцент эпифиза открывает дорогу элевационным, растормаживающим процессам перестроек в гипоталамусе. В свою очередь, появление этих провоспалительных модификатов действует подавляюще на пинеалоциты, что может стать индуктором сигналинга для запуска новых программ зрелости и перехода на новые, следующие этапы онтогенеза. В частности, эти модификаты могут повышать резистентность в таких высших регулировочных центрах, как эпифиз и гипоталамус, с переходом-перестройкой на новые принципы регулировок для реализации новых этапов онтогенеза. Эпифиз отключается, а гипоталамус отключает одни ядра-центры регулировок, но разблокирует, запускает, активирует другие.
Аналогия процессов сочетания сенесцента (возникает в иммунных клетках эпифиза) и сенилита (в функциональных пинеалоцитах стем-клетках эпифиза) происходит и во всех других тканях организма
Новые модификаты (не фенотипы) иммунных клеток, вместо того чтобы обслуживать и обеспечивать трофику (иммунометаболизм), становятся антагонистами для своих стем-клеток (например, для пинеалоцитов), подавляя или истребляя их.
Как вывод можно уточнить, что иммунные клетки микроглии настроены на уровень одних гормонов (соматотропного, гонадотропных…), тогда как иммунные клетки-резиденты в других тканях настроены на другие сигналинги, которые у каждого вида тканей различны. Следовательно, эти резиденты представлены изначально для каждого вида ткани и запрограммированы на специфичное сенсорное восприятие уровня их функционирования. Это означает, что у каждого типа резидентов есть свои специализированные сенсоры на контроль и регулировку активности клеток-функционеров. Клетки-резиденты одной ткани не могут заменять резидентов другой ткани. Итак, резиденты имеют специализированные сенсоры для контроля каждого типа тканей.
Преждевременное старение эпифиза — пролог для преждевременного старения и анизомалий организма
Стало понятно, что старение (инволюция) эпифиза реализуется через сенесцент его иммунной системы. Известно, что старение эпифиза может начаться и в 10 лет, и в 15–16 лет. У животных-короткожителей инволюция эпифиза начинается в возрасте 1–2 года, а у долгожителей — растягивается на многие годы. Чем позже начинается половая зрелость, тем «на позже» отодвигаются анизомалии*. Иммуностарение играет ключевую роль в развитии не просто большинства хронических заболеваний у пожилых людей, а именно возраст-зависимых, которые и являются его проявлением.
Омоложение через эпигенетические механизмы на клеточном уровне через эпифизарно-тимусную иммунную ось
Стареющая иммунная система как стартер для появления сенесцентных клеток
Основные органы, где нахождение и активность стволовых клеток максимальна:
- селезёнка;
- костный мозг;
- спинной мозг;
- яичник у женщин, придатки яичек — у мужчин.
Степень участия у всех одинакова.
Однако же командует этим производством только вилочковая железа. По мере уменьшения энергетики эфирного органа тимуса его команды со временем слабеют.
Регулировки в организме осуществляются двухэтажно. Эпифиз и мелатонин поддерживают юность всех иммунных клеток. Но автор предлагает концепт о наличии общей стороны эпифизарно-тимусной иммунной системы для поддержания ювенильности. Согласно исследованиям, молодые иммунные клетки противодействуют старению организма, в то время как сенесцентные иммунные клетки, наоборот, способствуют этому процессу [4].
Удаление тимуса ускоряет старение организма. После удаления органа риск смерти от различных причин повышается почти в три раза [5]. В молодости тимус поддерживает ювентал клеток, а в более зрелом возрасте противодействует аутоиммунным, раковым и анизомалийным заболеваниям. Удаление тимуса, согласно исследованиям, происходило на взрослых людях, когда размеры тимуса уменьшены в десятки раз. Это говорит о том, что у тимуса в юном возрасте должна быть особая миссия, связанная с поддержанием ювентальности.
Удаление тимуса в детском возрасте приводит к преждевременному старению иммунной системы
Без тимуса у взрослых увеличивается вероятность развития аутоиммунных заболеваний и рака. Очевидно, такое резкое повышение смертности от «всех видов болезней» связано с реализацией механизмов анизомалий* и повышением степени сенесцентности. Проще говоря, ослабевает Жизненная Сила на клеточном уровне, а количество сенесцентных клеток начинает доминировать над ювентальными.
Показано, что стареющая иммунная система не только допускает накопление сенесцентных клеток, но и сама способна «подталкивать» клетки к старению. Значит, тимус, как и эпифиз, — это ещё один как анти-, так и просенесцентный регуляторный орган, а в целом это единая система регулировок сенилита и юности. Тимус чётко увядает с наступлением пубертата, гормональной зрелости. Но при подавлении его антисенесцентной функции запускаются механизмы сенесцента и во всех других тканях.
У евнухов может отсутствовать инволюция тимуса (атрофия) в связи с отсутствием половых гормонов.
Согласно этой гипотезе, в результате может увеличиваться продолжительность жизни евнухов. Так, исследование о придворных евнухах династии показало, что продолжительность жизни евнухов была на 15–20 лет больше, чем у мужчин с нормальной репродуктивной функцией, живущих в тех же условиях.
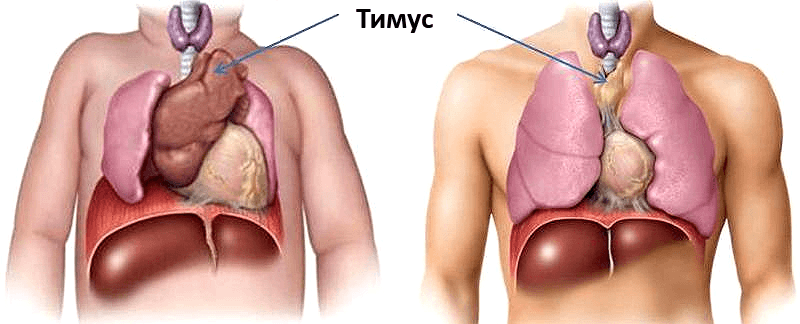
Рис. 1. На рисунке для сравнения приведены размеры тимуса у ребёнка (новорождённого) и у человека 50 лет. По размерам тимус соизмерим с другими важными органами, такими как печень, лёгкие и др. Эти огромные размеры явно показывают, что у тимуса, кроме иммунной функции, есть и другая — трофическая (иммунометаболическая), а точнее — поддерживать ювентальность иммунных клеток. Наука пока об этом молчит и не догадывается
Предназначение фетальных белков — защита плода от иммунного отторжения! Они делают иммунитет матери толерантным (терпимым) к антигенам. Но участвуют ли он в поддержании ювентальности клеток? Ясно, что омоложение матери не происходит (нет парабиогенного эффекта*).
Альфа-фетопротеин (AFP). Преобладающий сывороточный белок плода, который после рождения уступает место альбумину. AFP участвует в регуляции внутриклеточных механизмов роста и гибели клеток, а также снижает иммунологическую реактивность аллогенных лимфоцитов.
Таким образом, нельзя путать фетальные белки с UASP* — комплекс веществ, поддерживающих ювентальность* клеток и противодействующих SASP*.
Но есть сведения о некоторых белках (не AFP), которые играют важную роль в раннем эмбриональном развитии, например:
- Oct3/4. Белковый транскрипционный фактор семейства гомеобокс, который необходим для поддержания плюрипотентности стволовых клеток.
- Sox2. Белковый транскрипционный фактор семейства SOX, который связывается с малой бороздкой ДНК и также играет решающую роль в раннем эмбриональном развитии и самоподдержании популяции клеток.
Очевидно, ювентальность является результатом изначальной внутренней настройки популяций всех иммунных клеток на ювентальность (см. ниже кейлонную* гипотезу системы саморегуляции популяций клеток).
Автор предлагает выделить такие девственные модификаты ювентального типа и обозначить как Mu, чтобы затем отличать их от модификатов сенесцентных, и обозначить как Мs. Очевидно, через некие кейлонные белки и UASP эти иммунные девственные клетки «регулируют» все остальные иммунные клетки-резиденты данной ткани, а те в свою очередь влияют на активность или подавление стволовых клеток каждой ткани. Это аналогично тому, как сенесцентные клетки «заражают» своим белком другие клетки. Они содержат белок ReHMGB1. Молекула начинает воздействовать на рецепторы соседних клеток, и те, в свою очередь, тоже «заражаются» процессом старения. Итак, есть белки ювентальности, а есть белки сенесцентности?
Но как клетки Mu узнают, что надо перейти в Ms, если для этого нет внешнего сигналилинга? Регулировка таких тканей происходит сугубо изнутри, согласно принципам существования клеточных популяций на основе саморегуляции и самоограничения роста. Морфогенез и саморегуляция ткани в целом основаны на этих же принципах, являющихся по сути ансамблем различных популяций с учётом взаимосаморегулировки в ней всех клеточных популяций. Каждая популяция, будучи автономной, в то же время соподчинена требованиям ткани. Каждый орган состоит в свою очередь из ансамбля тканей, тоже существующих на правилах саморегулировки.
Кейлонная концепция системы саморегуляции даёт объяснение тканевым гомеостазам [1]. В этом случае ткань изнутри знает, до каких размеров ей расти и сколько циклов клеточного деления надо пройти, а также знает (коммитирована), когда надо остановить рост и запустить механизмы сенесцента. В данном случае сенесцент является механизмом, через который реализуются эти регулировки.
Это означает, что сенесцент может запускаться как сверху, так и исходить снизу по правилам кейлонной саморегулировки гомеостазов ткани. Кейлоны — это вещества и гены, регулирующие рост ткани.
Очевидно, известный лимит Хейфлика (ограниченного числа репликаций клеток до 52) тоже связан с этими кейлонными саморегулировками. Клетки в культуре ткани — это то же самое, что вырванный из контекста текст, работают на принципах культур самоограниченных по размеру и числу репликаций. Таких коммитаций или самоограничений в растительном мире нет. Но те же клетки в составе ткани и организма могут работать уже по другим правилам.
Инволюция тимуса — проявление программы старения или программы развития? Автор позиционирует ювенильный тимус как орган поддержки ювентальности иммунных клеток и среды крови. Детский тимус максимально способен к парабиогенезу, то есть обеспечивает мощную доминантность ювентальности над сенесцентом. Очевидно, вытяжки ювенильного тимуса будут противодействовать лимиту Хейфлика, когда клетки in vitro способны к репликациям около 52 раз.
Ряд данных свидетельствуют, что эпифиз является органом иммунной системы, а верифицированные в нём иммунные клетки могут выполнять компенсаторную роль при возрастной атрофии тимуса [7]. Но, с другой стороны, известно, что мелатонин способен активировать вилочковую железу (тимус) и стимулировать иммунитет. С угасанием эпифиза угасает и тимус. Обращает на себя внимание, что тимус, как и эпифиз, угасает в юности и даже детстве. В обоих этих органах происходит инволюция, вырождение. Расцвет юности возможен только в условиях максимальной активности эпифиза и тимуса.
Для внутренних процессов человеческого организма характерны совершенно иные темпы изменений. «Возрастной порог» нашей иммунной системы расположен гораздо ближе к детству, чем к старости. Уже с первого года жизни в тимусе ребёнка начинают происходить драматические изменения: функциональная ткань органа заменяется на соединительную, уменьшаясь каждый год на 3 % до 35–45 лет, а после 45 — на 1 %. В 70 лет соединительная ткань занимает 90 % тимуса [8]. Наиболее активно тимус функционирует в пренатальный период и до наступления половой зрелости.
Автор выдвигает концепт, что это связано с тем, что тимус в юности, кроме иммунных функций, также вместе с высоким уровнем мелатонина ещё поддерживает определённый статус ювентальности иммунных клеток. И в этом ему помогает мелатонин эпифиза. Это означает, что эпифиз и тимус — это составные единой системы, у которых имеется, кроме других функций, одна общая сторона взаимодействия — поддерживать ювенил и ювентал.
Кроме поддержки ювентальности, тимус противодействует онкологическим процессам. Дело в том, что сенесцент и онкология имеют много общих механизмов. Автор считает, что возрастная онкология — это одно из проявлений сенесцента. Оказывается, тимус участвует в защите организма человека и от рака. Показано, что тимус имеет решающее значение для здоровья взрослых в целом, а также для предотвращения рака и, возможно, аутоиммунных заболеваний.
При этом эпифиз поддерживает на общеорганизменном уровне и противостоит сенилиту за счёт ювенила, тогда как тимус работает на клеточном уровне иммунитета и противостоит сенесценту за счёт ювентала.
Люди с прогерией (преждевременное старение) живут намного меньше. Также показано, что прогерия связана с изменениями в тимусе, при этом заболевании наблюдается инволюция тимуса (уменьшение его размеров)! Это важнейший аргумент того, что сенесцент и сенилит начинаются с тимуса. Продолжительность их жизни колеблется от 7 до 28 лет, в среднем составляя 12–13,5 года [9]. Основные причины летальных исходов — острый инфаркт миокарда, застойная сердечная недостаточность, инсульты на почве атеросклероза — типичные преждевременные анизомалии.
Но это же означает и обратное: чем дольше сохраняется юность тимуса, тем дольше организм не стареет. Согласно мнению многих учёных, сохранение функции тимуса может продлевать молодость организма. Темпы старения сопряжены с тимусом и иммунной системой.
Также выявлено, что в зависимости от возраста наступления первой менструации у девочек зависит проявление скорости наступления болезней возраста (анизомалий). Этот момент (возраст запуска менархе) может быть настоящей «лакмусовой бумажкой» её будущего здоровья. Женщины, у которых менархе (первая менструация) случилось до 10 лет, в зрелом возрасте гораздо чаще страдали от ожирения, гипертонии, диабета, сердечно-сосудистых заболеваний и осложнений во время беременности (например, преэклампсии). Все эти возрастные проблемы одновременно являются не только гормонозависимыми, но и иммунозависимыми. А вот тем, у кого первая менструация началась позже 15 лет, повезло чуть больше с весом — риск ожирения у них был ниже. Но! Увеличивалась вероятность нерегулярного менструального цикла. Очевидно, что раннее менархе связано с ускоренным старением тимуса и эпифиза, а значит, и ускоренным старением всего организма. Неотенические типы живут дольше. Ускорение старения эпифиза усиливает элевацию гипоталамуса.
Идеальное Здоровье — это не только крепкий иммунитет, но и гормезис, которые возможны только в молодости, юности.
Самый высокий пик показателей Витаукта и Жизненной Силы — в период становления пубертата. Именно в этом возрасте самая мощная поддержка от врождённого и приобретённого иммунитета, которые и «открывают дверь» в сторону иммуноювентализации, или к иммуностарению. Приобретённый иммунитет — это по сути клонотипический иммунитет (резистентность — нечувствительность), ответственный за «иммуносенсибилизацию» (иммуносенесценция) — процесс ослабления иммунитета, который возникает с возрастом на ряд специфических и неспецифических факторов экзогенной природы. Это проявляется в уменьшении производства новых лимфоцитов в костном мозге и тимусе, а также в снижении способности иммунных клеток распознавать и уничтожать возбудителей. Но таковыми могут стать и факторы эндогенного характера, сопряжённые с сенесцентом и иммуностарением. Среди них эпигенез и онтогенез, исключающие ювентальность клеток и ослабляющих их Жизненную Силу.
Как итог резкое повышение заболеваемости и смертности. Причины смерти у пожилых людей чаще, чем у людей в возрасте от 25 до 44 лет: рак — в 43 раза чаще, пневмония и грипп — в 89 раз чаще, болезни сердца — в 92 раза чаще, а инсульт и хронические заболевания лёгких — более чем в 100 раз чаще!
Механизм иммуносенесценции:
- Сокращение количества наивных Т-лимфоцитов — накопление клеток памяти не компенсирует эту утрату, снижая адаптацию к новым патогенам.
- Накопление миелоидных клеток-супрессоров и позднедифференцированных Т-клеток.
- Снижение цитотоксической активности иммунных клеток, а также экспрессии функциональных молекул, связанных с цитотоксической активностью (гамма-интерферон, гранзим B и перфорин).
- Изменение метаболизма иммунной системы: повышенный гликолиз и выработка активных форм кислорода, снижение синтеза митохондрий.
Причины: сенесцент и сенилит.
Возраст — это всегда высокая активность зрелого гипоталамуса, который находится в противофазе с ювентальностью тимуса и ювенильностью эпифиза. Зрелый гипоталамус всегда будет их подавлять и доминировать над ними. Следовательно, высокая ювентализирующая активность тимуса и ювенилизирующая эпифиза возможны только в возрасте юности, до пубертата. Поддержание максимального здоровья и долголетия на фоне сохранения зрелости организма невозможно.
Эпифиз — основа Витаукта в юности, а тимус — база Жизненной Силы, то есть ювентальности клеточного уровня. Максимальный накал Витаукта и Жизненной Силы — это допубертатный период, то есть ранняя юность (но не детство). Также они интегрированы на гормезис и гомеостазы. Следовательно, максимальное проявление Витаукта и продление жизни возможны только на этапе ювенил. Это означает, что высочайшая мощь Витаукта для продления жизни возможна только при поддержании статуса неотении*. Только здесь возможно обеспечить высшую эффективность здоровья. Кстати, неотения не означает отсутствие репродуктивных способностей и инфантильность. Аксолотли, сохраняющие неотению, тем не менее легко размножаются.
Все эти процессы с возрастом движутся, изменяются посредством механизмов гормезисорезов* и гомеостазорезов*. Все остальные этапы после юности — это неизбежное отодвижение, удаление от здоровья, то есть выход из зоны оптимума как для Витаукта, так и для Жизненной Силы. Чем слабее Жизненная Сила (ювентальность), тем слабее Витаукт (ювенильность), и наоборот, чем слабее Витаукт, тем слабее Жизненная Сила. Витаукт — это сугубо прерогатива юности. Крайними антиподами для них являются сенесцент и сенилит.
Первично процесс старения начинается на уровне Жизненной Силы, то есть посредством сенесцента. Начинается этот процесс в юности и пубертате, когда угасают-подавляется тимус, а затем эпифиз. Вместе с этим ослабевает и их миссия по ограничению гиперфункции и перепрограммированию иммунных клеток. В крови появляются SASP*, которые приобретают решающую значимость вместо UASP*, а также «зрелые» иммунные клетки, которые перепрограммированы и отличаются от тех, что были до пубертата. Это происходит в связи с изменением гормонального профиля, в частности на фоне усиления половых гормонов и снижения уровня гормонов роста. Мощь Витаукта резко возрастает, но без обеспечительной поддержки со стороны Жизненной Силы. Усиление основной мощи Витаукта перераспределяется в репродуктивном направлении.
Витаукт в это время находится в расцвете, апогее, и он ещё долго будет поддерживать организм, вплоть до зрелости и адальтуса*. Но при этом происходит перекос — доминирование Витаукта над Жизненной Силой. Потребности отстают от возможностей. Но долго такое доминирование существовать не может. Разрыв в балансах этих процессов ведёт к истощению Витаукта, ослаблению его возможностей. Такие ограничения, в свою очередь, ведут к ослаблению потенциала поддержки для Жизненной Силы, он тоже слабеет за счёт перекоса между SASP и UASP, нарастания процессов онтофизиса* и эпигенеза. Идёт медленное уменьшение потенциалов то Витаукта, то Жизненной Силы. Эта раскачка идёт волнами, ступенчато, пока организм не пройдёт весь свод разных периодов, этапов-ступеней на онтодианной линии. Именно это взаимоослабление одного уровня другим является драйвером онтогенеза, ведущего к геронтосу и мортусу. Это когда становится невозможной поддержка Витаукта для Жизненной Силы и наоборот.
Эпифиз реализует свои задачи по продвижению по онтодианной линии (созревание организма на верхнем и нижнем уровнях в сторону от ювенила, пубертата к адальтусу… сенилиту) посредством настройки тимуса. Но тимус своей активностью тоже модулирует эпифизарный иммунный камертон. Запустить сенесцент микроглии эпифиза могут сигналы со стороны тимуса.
Тимус — один из первых органов, где начинают регистрироваться возрастные изменения негативного характера. С возрастом масса тимуса уменьшается, его корковый слой замещается соединительной тканью. Максимальный уровень выработки гормонов тимуса наблюдается в раннем возрасте — до начала полового созревания.
Выявлены вещества, такие как BMP4 и активин, которые являются факторами роста и дифференцировки, ключевыми в самообновлении и дифференцировке эпителиальных стволовых клеток тимуса, и изменение их уровней в результате старения вызывает потерю этих эпителиальных клеток. Эта потеря в результате приводит к снижению производства Т-клеток в тимусе, что в конечном итоге оставляет нас открытыми инфекциям и болезням. Это исследование является первым в мире и выявляет основную причину, по которой мы испытываем потерю эпителиальных стволовых клеток тимуса, а также молекул и механизмов, которые управляют этим процессом.
Иммуносенесценция — конечным результатом этого процесса является то, что наше тело больше не может обеспечить эффективную защиту от болезней, неправильно активируется, что приводит к иммунной дисфункции и хроническому воспалению. Уменьшение тимуса связано с риском развития рака, который резко возрастает с возрастом, согласно концепции иммуносенесцентного рака. Иммунное старение также сильно коррелирует со множественными возрастными патологиями.
Эпифиз тоже претерпевает возрастные изменения: угасание эпифиза начинается после наступления пубертата. Это указывает на то, что эпифиз подчиняется сигналам тимуса на сенесцент. У пожилых людей наблюдается атрофия паренхимы эпифиза, в которой локализованы мелатонинсинтезирующие пинеалоциты. При этом у 29 % пожилых людей функциональная активность эпифиза не снижается, и высокий уровень секреции мелатонина может способствовать восстановлению функций тимуса даже при значительных инволютивных изменениях. Эти данные указывают на то, что можно целенаправленно давать длительно (6 и более месяцев) взрослому человеку высокие дозы мелатонина (25 мг/сутки), что поможет восстановить и поддержать высокий уровень работы тимуса, что, в свою очередь, со временем само приведёт к активации эпифиза. Активность эпифиза сдерживает половую зрелость, а затем и сенилит… Через механизмы обратной связи это продлит юность тимуса......
Читать далее.... https://disk.yandex.ru/d/PeDAcUdzrCXtBg
- Доставка почтой России
- Курьерская доставка (до двери)
- Доставка транспортной компанией (СДЭК, Boxberry, ЦАП, Деловые Линии)
- Самовывоз по адресу г.Сочи, ул. Северная 6.
Обратите внимание, что у Почты России есть три тарифа: Обычная доставка, Ускоренная и EMS.
Ускоренная – на 80-100% дороже, в среднем посылка приходит на 2-3 дня быстрее.
EMS – доставка посылки до двери.
Вопросы по доставке вы можете задать по телефонам:
+7 (938) 467 78 06
+7 (928) 234 98 80
+7 (995) 003 74 85
Стоимость доставки
При заказе обычной доставки почты России у нас действует система скидок. Чем больше ваш заказ, тем ниже стоимость доставки. Обратите внимание, акция действует только на территории РФ.
Сумма заказа
|
Сумма заказа |
Стоимость доставки |
|
До 800 рублей |
350 |
|
От 800 до 3500 рублей |
300 |
|
От 3500 до 5000 рублей |
250 |
|
От 5000 |
Бесплатная доставка |
При ускоренной доставке Почты России, EMS или транспортной компании, Вы оплачиваете фактическую стоимость доставки. Она зависит от расстояния и размера заказа. Стоимость доставки рассчитает наш сотрудник, который с Вами свяжется.
- Переводом на карту Сбербанка 2202 2082 1192 6689, владелец Геннадий Алексеевич Гарбузов. Платеж можно сделать с помощью приложения Сбербанк Online, через банкомат или в отделении Сбербанка (все варианты без комиссии). Или переводом с карты другого банка (размер комиссии уточняйте в вашем банке)
- Произвести оплату с вашей банковской карты при оформлении заказа (через сервис Robokassa)
- Произвести оплату с вашей банковской карты по выставленному счёту (через сервис Robokassa).
- Оплатить с помощью платёжных систем Золотая Корона (для жителей СНГ), Western Union и MoneyGram (для жителей дальнего зарубежья)
- Возможны иные способы оплаты по согласованию с вашим менеджером.
Обратите внимание! Заказы мы отправляем только по предоплате. Если Вам по какой-то причине это неудобно, мы готовы пойти на компромиссный вариант: Вы внесёте частичную небольшую предоплату, а остальную сумму оплатите при получении посылки.
Возврат или обмен товара, который не подошел (не понравился), допускается, если с момента покупки прошло не более 7 дней (статья 26.1, пункт 4 ЗоЗПП) и он не входит в перечень товаров, не подлежащих возврату и обмену. Для проведения операции нужно позвонить по номеру +7(495)744-63-63 или отправить письмо на электронный адрес vitauct8@yandex.ru.
Обменять или вернуть товар можно в течение недели, если соблюдены условия:
- товар не использовался, не вскрывался;
- упаковка не повреждена;
- не нарушены технические, лечебные, другие свойства товара;
- сохранен товарный вид изделия;
- присутствуют ярлыки, пломбы;
- есть документация на продукцию, чек на покупку.
Обмен производится однократно на аналог такой же стоимости (без перерасчета) или на более дешевый/дорогой аналог с перерасчетом стоимости и возвратом/доплатой.
При отказе от заказа Garbuzov.org обязуется вернуть уплаченную по договору сумму в течение 10 дней со дня предъявления требований по возврату, за исключением расходов на пересылку товара, которые оплачивает покупатель (статья 26.1). При ненадлежащем качестве продукции продавец берет на себя транспортные расходы в оба направления.
При 100 %-ной оплате заказ нужно получить до истечения срока хранения. Если заказчик не забирает посылку в установленные сроки хранения, товар возвращается отправителю. Транспортные расходы в этом случае оплачивает заказчик.
Подробную информацию можно узнать здесь.








Попробовали? Оставьте отзыв